סרטן השחלות הוא ממאירות המהווה כ-25 אחוז מכלל הממאירויות הגינקולוגיות. שכיחותה של מחלה זאת באוכלוסיה הכללית מגיעה ל-1.5 אחוזים (אחת ל-70 נשים). על פי מרשם הסרטן הלאומי, מתגלות מדי שנה בישראל
כ-300 חולות חדשות עם ממאירות שחלתית.
מחלה זאת מהוה אתגר טיפולי לכל מרכז רפואי המתמודד עם חולות אלו לאור העובדה כי מעל לשני שלישים מהחולות מתגלות בשלב מתקדם של המחלה
(Advanced disease), שלב שבו קיימת מעורבות גרורתית של איברים מחוץ לאגן ובעיקר בבטן העליונה (תרשים 1).
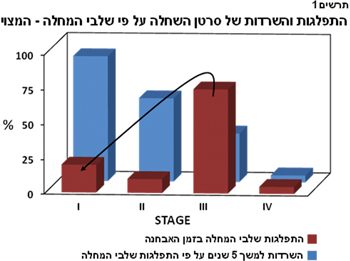
האגרסיביות של מחלה זאת באה לידי ביטוי בעובדה שבממוצע רק 25-20 אחוז מהחולות המאובחנות מצליחות לשרוד למשך חמש שנים או יותר (תרשים 1). הסיבה לנוכחות מחלה מתקדמת בשלב האבחנה של מרבית החולות עם סרטן השחלות נובעת בעיקר מהעדר תסמינים קליניים בשלביה הראשונים של המחלה וזאת בניגוד לממאירויות מקבילות, דוגמת סרטן הרחם או סרטן המעי שבהן מופיעים תלונות קליניות כבר בשלבי המחלה הראשוניים, מה שמאפשר גילוי וטיפול במצבים ממאירים אלה בשלבים טרום ממאירים או בשלבים מוקדמים.
לאחרונה פורסמו שבעה ממצאים קליניים אשר דווחו על ידי חולות סרטן השחלה כתסמינים מקדימים לפני האבחנה הסופית של ממאירותן. תסמינים אלה כללו: כאבי בטן, נפיחות בטנית, מתיחה של דופן הבטן, תלונות אורינאריות, ירידה בתיאבון ודימום רקטאלי. למרות הגדרת תסמינים בלתי ספציפיים אלה, בחישוב יכולת הניבוי החיובית לנוכחות סרטן השחלות על פי מקבץ התסמינים המתואר (positive predictive values) נתקבל ערך חיזוי נמוך אשר הגיע לאחוז עד שני אחוזים בלבד1.
בנוסף, חוסר ידע לגבי מצבים טרום ממאירים של סרטן השחלות, כמו גם העדר שיטה יעילה לביצוע סקר אוכלוסיה לגילוי מוקדם של סרטן השחלות (דוגמת המצב בממאירות צוואר הרחם), אחראיים לאבחנה המאוחרת של ממאירות אגרסיבית זאת.
המאמצים לפתרון מצב זה מתמקדים בשני כיווני מחקר: הראשון, ניסיון לאתר סמנים ראשוניים, בדיקות סקר יעילות לגילוי מוקדם של סרטן השחלות וזיהוי אוכלוסיות בסיכון מוגבר לחלות בממאירות זאת. סקר יעיל עשוי לשפר את אחוז החולות אשר מתגלות בשלב התחלתי של המחלה ולהסיט את עקומות גילוי המחלה לשלבים מוקדמים יותר ובכך לשפר את עקומת ההישרדות מסרטן השחלות כפי שמודגם בתרשים מס' 2.
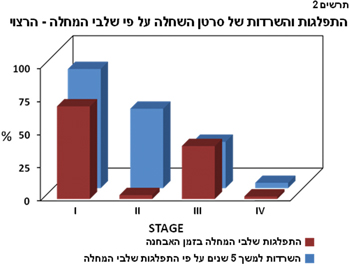
קו המחקר השני הוא ניסיון לפתח תרופות יעילות יותר, פרוטוקולים מורכבים יותר ושילובים שונים בין הכירורגיה לתוספות הכימותרפיות בטיפול בממאירות אגרסיבית זאת.
חידושים ושינויים בטיפולים העכשוויים
הטיפול בסרטן השחלות כולל שילוב בין טיפול ניתוחי אגרסיבי לטיפול כימותרפי המשלב לרוב מספר תרופות ציטוטוקסיות (כימותרפיה).
מאז הוחל בשימוש בתרכובות פלאטינום לטיפול כימותרפי בסרטן השחלות (לפני כ-30 שנה), לא דווח על שיפור משמעותי בהצלחות הטיפול בממאירות זאת, כפי שבא לידי ביטויו במשך תקופת הרמיסיה ((Progression - Free Survival או בסך כל החיות לאחר אבחנת המחלה (Overall (Survival.
לאחרונה אנו מדווחים על ניסויים קליניים מתקדמים שמטרתם לנסות ולשפר את תוחלת ואיכות החיים של חולות סרטן השחלות. מחקרים אלה הם ברובם פרוספקטיביים עם רנדומיזציה כפולת סמיות ומבוקרת, מה שנותן לתוצאותיהם כוח סטטיסטי ודרגת מהימנות גבוהה.
כיווני מחקר ושינויים אלה כוללים ארבעה ממדים: הראשון, המעבר לטיפול ניאואדגובנטי במצבים של מחלה שחלתית מפושטת. השני, שימוש במתן כימותרפיה לתוך חלל הצפק. השלישי, תוספת תרופות ביולוגיות. הכיוון האחרון הוא המחשבה למתן טיפול תמיכתי (maintenance) במהלך הרמיסיה מהמחלה.
טיפול ניאואדגובנטי - בחודש נובמבר 2008 פורסמה עבודה פרוספקטיבית אירופאית שהשוותה את יעילות הטיפול המקובל בסרטן שחלה מתקדם, הכולל כירורגיה נרחבת השואפת להסרה מקסימלית של הרקמה הגידולית ולאחריה תמיכה כימותרפית אדגובנטית (בתכשירי פלאטינום ובטקסול). זרוע "מסורתית" זאת הושוותה לזרוע המחקר שכללה טיפול כימותרפי ראשוני (ניאואדגובנטי) שכלל שלושה קורסים ולאחריו כירורגיה המכוונת להסרת כל השארית הגידולית ובהמשך השלמת הטיפול הכימותרפי (שוב שלושה קורסים)2.
תוצאות עבודה זאת הראו הישרדות ותקופות העדר מחלה זהות בשתי זרועות המחקר, עם תחלואה ניתוחית נמוכה יותר בצורה משמעותית מבחינה סטטיסטית בזרוע אשר נחשפה קודם הניתוח לכימותרפיה (הזרוע הניאואדגובנטית). תוצאות אלו הביאו לשינוי בקביעת מדיניות הטיפול הראשונית בחולות עם סרטן שחלה מתקדם.
שינוי מעשי זה הביא למספר התנהלויות שונות בטיפול היומיומי בחולות עם סרטן שחלות מתקדם. שינויים אלה כללו: א. שימוש וצורך לבצע ביופסיות מרקמת הגידול לפני ההחלטה על מתן כימותרפיה. ב. הכוונת החולות לטיפול כימותרפי מקדים לפני הטיפול הכירורגי הנרחב. ג. הקטנת ההיקף הניתוחי. כלומר, ירידה בצורך בביצוע כריתות מעי ושאר איברי בטן ואגן במטרה להשיג כריתה גידולית אופטימלית.
יצוין כי גישה טיפולית חדשה זאת לא הראתה שיפור בתוצאות הטיפול אך הקטינה באופן משמעותי את התחלואה הניתוחית המתלווה לטיפול בסרטן השחלות המתקדם ואפשרה לחזור לטיפול כימותרפי ללא עיכובים משמעותיים, תוך שמירה על איכות חיים טובה יותר של המטופלות.
טיפול כימותרפי ישיר לחלל הצפק - לעומת הטיפול הניאואדגובנטי אשר לא הראה שיפור בהישרדות של חולות סרטן השחלות, עבודות פרוספקטיביות של מתן טיפול כימותרפי ישירות לחלל הצפק הראו שיפור בהישרדות מממוצע של 49.5 חודשים ל-66.9 חודשים בחולות עם סרטן שחלות מתקדם, ולשיפור באורך הרמיסיה מהמחלה מ-19.3 חודשים ל-24.3 חודשים3.
יצוין כי הישרדות ממוצעת של למעלה מ-66 חודשים לא הושגה עד כה בשום פרוטוקול טיפולי אחר אשר כוון לטיפול בנשים עם סרטן שחלות מתקדם3.
יש לשים לב כי שיטת הטיפול התוך צפקית הראתה תופעות לוואי קשות באופן משמעותי יותר מאשר הטיפול הכימותרפי המקובל הניתן למערכת הסיסטמית. בנוסף, תועדה ירידה בולטת באיכות החיים של המטופלות אשר נחשפו לטיפול ישיר לחלל הצפק עם אחוזים גבוהים של הפסקת הטיפול (Drop out) בשל תופעות הלוואי וירידה באיכות החיים4,3.
במקביל חשוב להבין כי השיטה הוכחה כיעילה יותר רק לגבי חולות אשר עברו כירורגיה אופטימלית ראשונית, כלומר נותרו ללא כל שארית גידולית לאחר הטיפול הכירורגי הראשוני והיו מועמדות לטיפול כימותרפי בקו ראשון.
יעילות הטיפול מחד ותופעות הלוואי הקשות מנגד מביאות את הקלינאים לנסות ולחפש דרכים שונות (כמו הקטנת המינון, פיזור הטיפול בציר הזמן ושינוי התרופות הציטוטוקסיות הניתנות לווריד) וזאת כדי להקטין את התחלואה ולהגדיל את ההיענות לדרך טיפול זאת.
טיפול ממוקד לתהליך הגידולי (טיפול ביולוגי) - מאמץ מחקרי רב מושקע היום בניסיון להבין את שרשרת האירועים הביומולקולריים המתרחשים בתאי הגידול. הבנת אירועים אלה הביאה לפיתוח ולשימוש בתכשירים המשפרים את יכולת הטיפול בגידול הראשוני כמו גם שיפור בתגובה לכימותרפיה.
מספר תרופות ביולוגיות הוצעו כבעלות פוטנציאל לשיפור הטיפול בסרטן השחלות. אחד הכיוונים הנחקרים ביותר בתחום הטיפול בממאירויות בכלל ובסרטן השחלות בפרט הוא טיפול המתמקד בעיכוב התפתחות כלי דם לרקמת הגידול ((Angiogenesis Inhibition6. הטיפול מבוסס על הסימביוזה הביולוגית בין התפתחות רקמה ממארת לבין התפתחות כלי דם
(Neovascularization) שמטרתם לתחזק את ההתפתחות הגידולית. הנחת היסוד היא כי הפרעה באספקת הדם לרקמה הגידולית היא בעלת פוטנציאל לעיכוב הגידול הראשוני או עיכוב של התפתחות גרורות.
התרופות הפועלות במנגנון זה הן התרופות שתוקפות את גורמי הצמיחה של כלי דם (Antiangiogenetic Factors) או מעכבי גדילה של אנדותל הציפוי הפנימי של כלי הדם ((Anti-Vascular Endothelial Growth Factor. לקבוצת תרופות אלו שייכות תרופות כגון Bevacizumab (Avastin) ואף התרופה הישנה Thalidomide. בעבר הוכחו גורמים אלה כיעילים ואף הוכנסו לשימוש קליני בממאירויות המעי הגס, מלנומות וממאירויות אורינאריות6.
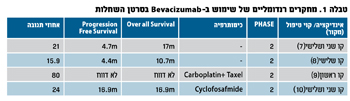
ארבעה מחקרים10-7 הראו תגובה קלינית לטיפול ב-Bevacizumab (Avastin) בממאירות שחלתית. תגובה קלינית זאת באה לידי ביטוי בעיקר בהערכה של התקופה ללא עדות לחזרת המחלה (Progression Free Interval) וזאת לאחר חזרת שניונית.
כיום מתנהל על ידי האיגוד האמריקאי לגינקולוגיה אונקולוגית מחקר פרוספקטיבי רנדומלי כפול סמיות (GOG 218) שמטרתו לבדוק אם תוספת של Anti-Vascular Endothelial Growth Factor לטיפול הכימותרפי הראשוני בסרטן השחלות שיפרה את תוחלת ואיכות החיים של החולות בסרטן השחלות. ממצאים ראשוניים ממחקר זה נותנים תקווה לשיפור בתגובה לטיפול הכימותרפי כמו הערכת תקופת הרמיסיה לאחר טיפול ראשוני זה.
תחום נוסף שמטרתו לשפר את התגובה לטיפול הכימותרפי בסרטן השחלות הוא הכוונת תרופות אשר מתערבות בתהליכי התיקון של ה-DNA התאי5.
תרופה המעכבת את האנזים Poly) ADP Ribose Polymerase) נמצאת כיום בניסוי קליני פרוספקטיבי בממאירויות השד והשחלות עם אפשרות לשיפור משמעותי של הטיפול הכימותרפי במצבים אלה11.
ההיגיון בטיפול זה הוא פגיעה ביכולת התיקון העצמי של תאים אשר עברו נזק סטרוקטוראלי בחומצות הגרעין שלהם - נזק אשר מתפתח במנגנון של חלק מהטיפולים הכימותרפיים. הטיפול במנגנון זה הראה השפעה ישירה על הרס תאים ממאירים כמו גם שיפור הפעילות הציטוטוקסית הנגרמת על ידי הטיפולים הכימותרפיים12.
התוצאות הקליניות הראשוניות בקבוצת תרופות אלו מצביעות על שיפור בתגובה לטיפול, בעיקר בקבוצת החולות הנשאיות למוטאציות בגנים 2-1BRCA וזאת לאור העובדה כי גנים אלה הם גנים המקודדים חלבונים המשמשים בתהליך התיקון של ה-DNA ומוטציות בגנים אלה חושפות את אוכלוסית הנשאיות לסיכון מוגבר לחלות בממאירויות השד והשחלות.
ממצאים אלה נותנים כיוון חדש המתבסס על התאמה טיפולית אישית לכל חולת סרטן השחלות על פי הגנוטיפ ועל פי הפרופיל הגידולי של החולה13.
טיפול מתחזק (Maintenance) וממאירויות שחלתיות - לאור העובדה שיותר מ-75 אחוז מהחולות בסרטן שחלות מתקדם יבטאו חזרה של מחלתן הבסיסית לאחר כ-18 עד 24 חודש בממוצע, נבדקה האפשרות למתן כימותרפיה מתחזקת (Maintenance Therapy) לאורך תקופת הרמיסיה הנרכשת לאחר הטיפול הראשוני14.
משך הטיפול המוצע נע בין שלושה חודשים לשנה וזאת במשך השנה הראשונה והשנה השנייה לאחר סיום הטיפול הכימותרפי ומיד לאחר השגת הרמיסיה15.
ההיגיון בטיפול זה מתבסס על טיפול בשאריות מיקרוסקופיות או במושבות גידול מתחדשות אשר לא ניתנות לזיהוי על ידי אמצעי ההדמיה או הסמנים הנמצאים כיום בשימוש קליני. טיפול זה אמור להאריך את זמן חזרת המחלה לאחר הכניסה לרמיסיה ראשונית.
לאחרונה הופסק המחקר הפרוספקטיבי של הקבוצה האמריקאית הדרום מערבית (SWOG)וה-GOG האמריקאי לאור ממצאי ביניים אשר הדגימו יתרון בולט של קבוצת המחקר אשר קיבלה טיפול כימותרפי מתחזק במשך 12 חודשים ואשר השיגה רמיסיה של 22 חודש בממוצע, לעומת קבוצת הביקורת אשר טופלה למשך שלושה חודשים בלבד והשיגה רמיסיה של 14 חודש
בלבד15. למרות ממצאים עכשוויים אלה (אוגוסט 2009), עדיין לא ברור אם תוספת הטיפול המתחזק האריכה את משך החיות של חולות סרטן השחלות Overall Survival ולכן יעילות הטיפול הנמשך למעלה משנה ופוגע באיכות החיים של המטופלות עדיין מוטלת בספק ומחכה לתוצאות של מחקרים ממושכים יותר העוקבים אחרי חולות אלו כמו גם לתוצאות מבחני איכות החיים של המטופלות וזאת לפני הכנסתה של גישה זאת לשגרת הטיפולים בסרטן השחלות.
לסיכום, ממאירות השחלות היא ממאירות אשר גם במאה ה-21 לא נמצא לה עדיין פתרון אופטימלי, זאת לאור העובדה שהמחלה מתגלה כשהיא במצב מתקדם. בנוסף לכך, לא חלה התקדמות משמעותית בטיפול ב-30 השנים האחרונות ולא נצפתה קפיצת מדרגה משמעותית באחוזי הריפוי או ההחלמה ממחלה זאת.
בארץ ובעולם מתמקדים מחקרים קליניים רבים בנסיונות למצוא דרך לגילוי מוקדם של המחלה כמו גם פתרון טיפולי אשר ישפר את תוחלת ואיכות החיים של חולות אלו.
קיימים היום מספר חידושים ושינויים בשגרת הטיפול בחולות סרטן השחלות: ראשית, המעבר לטיפול ניאואדגובנטי, טיפול לחלל הצפק או טיפול מתחזק. טיפולים אלה מתבססים על תשתית התרופות הנמצאות בשימוש שגרתי בטיפול בסרטן השחלות. המחקר הקליני מנסה גם לעשות שימוש בתרופות ביולוגיות חדשות אשר פוגעות נקודתית בתהליכים מקומיים באזור הגידול או בתהליכים תוך תאיים בתא הגידולי.
חידושים אלה והתפתחות כיווני הטיפול החדשניים הם תוצאה של ההתקדמות המחקר הבסיסי והמולקולרי אשר בבסיסו מכוון להבנת מנגנון ההתמרה הממארת בסרטן השחלות. הבנה זאת איננה מושלמת עדיין אך ההתקדמות בה היא רבה בעיקר בתת אוכלוסיות דוגמת הנשאיות ל-BRCA. ההתקדמות בהבנת חלק ממנגנוני ההתמרה הממארת מאפשרת לנו להכניס טיפולים ביולוגיים בניסיון להתמודד עם סרטן השחלות. שילוב טיפולי זה הוא דוגמה למגמה המתפתחת כיום בטיפולים אונקולוגיים אשר מתאימים באופן אישי את סוג הטיפול ומינונו למטופלת וזאת על פיה גנוטיפ ופרופיל הממאירות של החולה. גישה חדשנית זו מאפשרת לנו להאמין כי נמצא פתח להתקדמות משמעותית בתוצאות הטיפול במחלות אגרסיביות דוגמת סרטן השחלות.
ד"ר עופר לביא, מנהל היחידה לגינקולוגיה כירורגית ואונקולוגית, המרכז הרפואי כרמל, הפקולטה לרפואה ע"ש רפופורט, הטכניון חיפה, יו"ר החברה הישראלית לגינקולוגיה אונקולוגית