סרטן האשך הינו הגידול השכיח בגברים בגילאי 15-35, למרות היותו גידול נדיר באופן יחסי. היארעותו עומדת על 7,000 מקרים בשנה בארה"ב, לעומת 180,000 מקרים של סרטן ריאה ו-210,000 מקרים של סרטן הערמונית1.
מרבית גידולי האשך מקורם בתאי נבט, ורק בפחות מ-5 אחוז מהמקרים מדובר במקור תאי אחר. הסוגים הנפוצים ביותר של סרטן האשכים ממקור תאי נבט הם סמינומה וסוג שאינו סמינומה (התפלגות שווה). כמו כן, קיים סרטן אשכים, שהוא שילוב של שני הסוגים הללו. הסמינומה נפוצה בעיקר בגברים בגילאי 35-55, בעוד שגידולים שאינם סמינומה מופיעים בקרב גברים צעירים יותר (בגילאי 15-30).
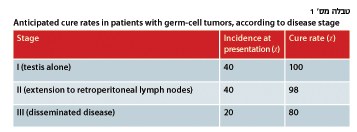
לעתים רחוקות, מופיעה באשכים לימפומה שאינה הודג'קין, כאשר הטיפול בסוג זה של סרטן הוא שונה ונעשה בהתאם לטיפול המקובל עבור לימפומה שאינה הודג'קין. למרבה המזל, גידולי אשכים הפכו לדוגמא של גידולים הניתנים לריפוי1,2. התערבות ניתוחית, טיפול כימותרפי המבוסס על תשלובת המכילה ציספלטין, קרינה או שילוב של הטיפולים, מובילים לריפוי באחוזי הצלחה גבוהים מאוד, הנעים בין 80-100 אחוז מהמקרים של גידולים ממקור תא נבט (ראה טבלה מס' 1).
זמינות סמנים מדויקים של הגידול בדמו של החולה הכוללים חלבון אלפא עוברי - alphafetoprotein)-AFP) והורמון גונדוטרופיני שלייתי אנושי
(hCG-human chorionic gonadotropin), מקלים על איבחון המחלה והמעקב הטיפולי בחולה. האנזים לאקטאט דהידרוגנאז (LDH-lactate dehydrogenase) הינו סמן פחות אופייני, אך גם הוא, בערכים מוגברים, מצביע על נפח המחלה3.
גורמי סיכון
הגורם לסרטן האשכים אינו ידוע. למרות שמדובר בסרטן נדיר, עולה שכיחותו בשנים האחרונות מסיבה שאינה ברורה. על פי רישום משרד הבריאות הישראלי, נרשמה עלייה מתמדת בשכיחות סרטן האשכים בין השנים 1980 עד 2002, המשקפת למעשה מגמה כלל עולמית. הסיכון לסרטן האשכים גבוה יותר בגברים צעירים לבנים, כאשר השכיחות הגבוהה ביותר נצפתה בסקנדינביה, שוויץ, גרמניה וניו-זילנד. שכיחות פחותה קיימת בארה"ב ובבריטניה ונמוכה אף יותר באפריקה ואסיה4-7.
גידולים אלו מתפתחים ב-1-2 אחוז מהגברים עם היסטוריה של אשך טמיר (cryptorchidism), כאשר סיפור עבר של טמירות אשכים בטנית מהווה סיכון גבוה יותר לעומת אשך טמיר מפשעתי. נתונים בספרות מצביעים על סבירות נמוכה להתפתחות סרטן האשכים במקרים בהם ניתוח הורדת האשך לשק האשכים מתבצע לפני הבגרות המינית. היסטוריה משפחתית של גידול זה מהווה גם היא גורם סיכון. בנוסף, סרטן אשכים קודם מעלה מ-1 ל-2 אחוז את הסיכון של גידול ראשוני באשך הנגדי2.
התייצגות קלינית
התסמין הנפוץ ביותר של סרטן האשכים הוא מסה חד צדדית בשק האשכים, ללא תלונות של רגישות או כאב. לעיתים, האבחנה הראשונית הינה שגויה והגידול מאובחן באופן מוטעה כדלקת של עילית האשך (epididymitis) או דלקת האשך (orchitis) והחולה מקבל טיפול אנטיביוטי. בהמשך, לעיתים קרובות מופיעים כאב ואי נוחות באשך החולה. חולים יכולים להתייצג עם תלונות של כאבי גב גוברים או כאבי בטן תחתונה, עקב מעורבות של בלוטות לימפה אחר צפקיות (רטרופריטוניאליות) בהתאם למיקום הגידול, כאשר סרטן של האשך השמאלי מתפשט לבלוטות לימפה אחר צפקיות שמאליות, וסרטן של האשך ימני בהתאם לצד ימין.
תסמינים נוספים של קשיי נשימה יכולים לנבוע ממעורבות ריאתית. הגדלת בלוטות לימפה על-בריחיות (supraclavicular lymphadenopathy) הינו ממצא שאינו שכיח, אך יכול להוות ביטוי של המחלה בהיעדר סימפטומים אחרים. לימפומה אשכית, השכיחה יותר מעל גיל 50, עשויה להתייצג עם תלונות סיסטמיות (כגון חום, הזעות, ירידה במשקל) ופיזור עם נטייה למעורבות מערכת העצבים המרכזית והאשך הנגדי8.
תסמינים אחרים כוללים: דדנות הזכר ((gynecomastia עקב רמה גבוהה של הורמון גונדוטרופיני שלייתי אנושי (hCG). הגדלה של בלוטות לימפה אחר צפקיות עלולה לחסום את השופכנים וכתוצאה מכך לגרום למיימת כלייתית (hydronephrosis) והפרעה בתפקוד הכלייתי. בנוסף, גידול המערב את המיצר מסוג שאינו סמינומה מלווה לעיתים ע"י תסמונת קליינפלטר (Klinefelter's syndrome) ובמקרים נדירים יותר אף לויקמיה מאגאקאריוכיטית חריפה (acute megakaryocytic leukemia), היכולים להופיע בשלבים מוקדמים או מאוחרים יותר של המחלה9,10.
אבחון ודירוג המחלה
בכל חולה עם חשד לממאירות של האשך, על הבדיקה הגופנית לכלול בדיקת אשכים, בטן, חזה ובלוטות לימפה על-בריחיות. בבדיקות המעבדה מלבד ס"ד וביוכימיה מלאה, יש לבדוק רמות AFP hCG ו-LDH. רמות גבוהות של AFP מצביעות על גידול ממקור שק החלמון או גידול אמבריונלי, רמות גבוהות של hCG אופיינות לכוריוקרצינומה וקרצינומה אמבריונלית. באחד מחמישה חולי סמינומה רמות hCG מוגברות בצורה קלה. במקרים של טרטומה טהורה (pure teratoma) הסמנים אינם מוגברים כלל.
במקביל לבירור המעבדתי, יש לבצע בדיקת על-שמע של אשכים, שמטרתה לאשר את נוכחות הגידול. סקרים רדיוגרפיים מוגבלים בדרך כלל לטומוגרפיה ממוחשבת של החזה, הבטן והאגן. בשלב זה, בדיקת PET-CT עדיין לא הפכה לבדיקת בחירה עקב שכיחות יחסית גבוהה של תוצאות כוזבות שליליות (false negative). עד 10 אחוז מגידולי תאי הנבט מופעיים באתר חוץ-אשכי8,2.
במקרים אלו, החולים בדרך כלל מתייצגים עם גוש בחלקו הקדמי של המיצר (בניגוד לגוש אחורי במיצר המאפיין גידול אשך גרורתי), או גוש אחור צפקי מרכזי (בניגוד לגוש אחור צפקי שמאלי או ימני, המאפיין גם הוא גידול אשך גרורתי). מאחר וגידול תא נבט המתפתח בחלקו הקדמי של המיצר אינו נובע מגידול אשך ראשוני, בדיקת על-שמע של האשכים אינה נחוצה. לעומת זאת, ישנו קשר הדוק יותר בין הופעת גידול באחורי הצפק (לכאורה ראשוני) ונוכחות גידול ראשוני סמוי באשכים. לכן, במקרים האלו מומלץ לבצע בדיקת על-שמע של האשכים. לאור זאת, באבחנה המבדלת של גידול ממאיר בגברים צעירים בדרגת התמיינות נמוכה, שמקורו לא ידוע, יש חשיבות מכרעת בהכרת האפשרות של גידולי תא נבט ראשוניים באתרים חוץ-אשכיים, מאחר והמחלה ניתנת לריפוי באחוזי הצלחה גבוהים1,2,8.
הערכה פתולוגית והיסטולוגית של הגידול מתבצעת על ידי ניתוח הסרת אשך (orchiectomy) בגישה מפשעתית. ניתוח זה - תפקידו ריפוי וגם אבחון. קיימת הוריית נגד לאבחון באמצעות ביופסיה דרך כיס האשכים, מאחר ופעולה זו מעודדת פיזור לימפטי מקומי והישנות מקומית של המחלה11,12. סרטן האשכים מאופיין על ידי סוג היסטולוגי יחיד או שילוב של הסוגים השונים של תאי הנבט (mixed germ cell tumor). כאמור, גידולי האשך מתחלקים לשני סוגים עיקריים: גידולים מסוג סמינומה וסוג שאינו סמינומה. הנוכחות של כל היסטולוגיה אחרת בנוסף לסמינומה תגדיר את הגידול כסוג שאינו סמינומה. רמה מוגברת של AFP בנסיוב הדם מצביעה על גידול מסוג שאינו סמינומה, גם בנוכחות סמינומה טהורה בבדיקה ההיסטולוגית2.
קביעת שלב המחלה וסיווגו בגידולי תאי נבט מתבססת על דירוג הכולל את היקף המחלה וסיווג פרוגנוסטי שלה ע"פ ההגדרות הבאות:
• שלב ראשון: גידול המוגבל לאשך.
• שלב שני: קיימת מעורבות של בלוטות לימפה אחורי צפקיות.
• שלב שלישי: מעורבות של הריאות או של איברים אחרים (מוח, כבד, עצם).
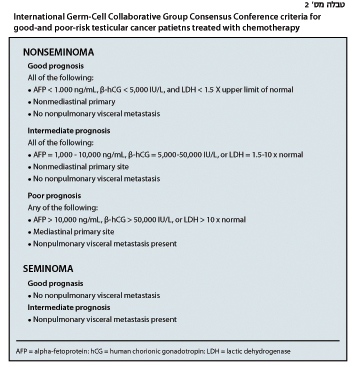
הסיווג הפרוגנוסטי של המחלה (ראה טבלה מס' 2) הינו חלק חיוני בהערכה הראשונית של החולה מאחר והוא מהווה גורם המשפיע על התוכנית הטיפולית המותאמת לכל חולה. הקבוצה הבינלאומית של סרטן בתחום גידולי תאי נבט The International Germ Cell Cancer) Collaborative Group-IGCCG) סיווגה בנפרד גידולים מסוג סמינומה (SGCT) וגידולים שאינם סמינומה (NSGCT) על פי גורמי הסיכון להישנות המחלה13. בגידולים שאינם סמינומה, גורמים פרוגנוסטים כוללים ערכים טרום טיפוליים של הסמנים; האתר הראשוני של הגידול (אשכים כנגד המיצר או אחורי-הצפק) ונוכחות גרורות וויסצרליות לא ריאתיות. בגידולים מסוג סמינומה, הגורם הפרוגנוסטי המשמעותי היחיד הינו נוכחות גרורות וויסצראליות לא ריאתיות, אשר מעניק דרגת סיכון בינונית (intermediate risk).
הטיפול בגידול מסוג שאינו סמינומה
לאחר השלמת הבירור הקליני והמעבדתי, הטיפול בגידולים מסוג שאינו סמינומה נקבע ע"פ שלב המחלה והסיווג הפרוגנוסטי, טוב ובינוני כנגד מופחת. גידול בשלב ראשון מטופל לעיתים קרובות באמצעות התערבות ניתוחית בלבד. לאחר הניתוח, סמני המחלה אמורים לחזור לערכים תקינים כ-3-4 שבועות לאחר כריתת האשך. זמן מחצית החיים של-hCG קצר (בין 18 ל-36 שעות), לעומת זאת זמן מחצית החיים של AFP נע בין 5 ל-7 ימים, לכן השגת ערכים תקינים יכולה לארוך מספר שבועות14,15. עם זאת, גם בחולים לאחר כריתת אשך המתייצגים עם ממצאים תקינים בטומוגרפיה ממוחשבת של החזה, הבטן והאגן ושל סמני הגידול, קיים סיכוי של 30 אחוז לנוכחות גידול מיקרוסקופי בבלוטות לימפה אחורי צפקיות או באתרים אחרים ולכן קיים סיכוי להישנות המחלה. למרות סיכוי משמעותי להישנות המחלה, קיים סיכוי אף גדול יותר לריפוי מלא לאחר התערבות ניתוחית בלבד בשלב מחלה זה. אי לכך, לחולים אלו על פי רוב מוצעות אפשריות הכוללות:
1) מעקב קליני צמוד בחולה ללא גורמי סיכון להישנות המחלה והיענות מלאה של החולה למעקב קפדני ביותר הכולל ביקורות מרפאה, בדיקות מעבדה ובדיקות הדמיה תדירות במשך מס' שנים.
2) טיפול כימותרפי משלים בחולה עם גורמי סיכון להישנות המחלה כגון חדירה לכלי דם וכלי לימפה ונוכחות של מרכיב אמבריונלי במעל מחצית מהגידול.
3) בתירה של בלוטות לימפה אחורי צפקיות (RPLND - Retroperitoneal lymph node dissection) וטיפול כימותרפי משלים. פעולה זו מתבצעת לאחר כריתת האשך ומאפשרת אבחנה פתולוגית מדוייקת של מעורבות בלוטות לימפה אזוריות והגדרת שלב הגידול בהתאם. בנוסף, פעולה זו מסייעת בהחלטה על השלמת טיפול כימותרפי. בחולים בהם בפעולה ניתוחית מסוג זה בלוטות הלימפה נמצאו חופשיות מגידול, הסיכוי להישנות מחלתם עומד על כ-10 אחוז. הישנות המחלה בקבוצה זו מאופיינת בעיקר על ידי הופעת גרורות ריאתיות.
במקרים של הישנות המחלה, על החולה להשלים שלושה מחזורי טיפול כימותרפי (כל מחזור כולל 21 ימים) הכולל תשלובת בליאומיצין (Bleomycin), אטופוסיד ((Etoposide וציספלאטין (Cisplatin) (BEP). בחולים בהם בלוטות הלימפה נמצאו מעורבות בתהליך הגידולי, קרי שלב מחלתם מתקדם יותר (שלב שני), וכך שכיחות הישנות הגידול עולה ונעה בין 30 ל-50 אחוז, בהתאם לגודל ומספר הבלוטות הנגועות. בחולים אלו, הטיפול האפשרי כולל מעקב קליני צמוד או טיפול כימותרפי בתשלובת BEP. תחת גישות טיפוליות אלו בגידול בשלב ראשון מושג ריפוי מלא ב-99 אחוז מהחולים1-3,16,17.
גידול בשלב שני של מחלה בעל נפח גדול (Bulky disease) או בשלב שלישי, מחייבים טיפול כימותרפי. המועמדים האופייניים הם חולים עם גרורות באחורי הצפק או גרורות ריאתיות בעת התייצגות המחלה, או לחלופין אלו בעלי רמות גבוהות של סמני גידול, שאינן חוזרות לערכים תקינים ב-3 עד 4 שבועות לאחר ניתוח לבתירת האשך. חולים בהם יש בלוטות לימפה אחורי צפקיות בקוטר הקטן מ-3 ס"מ, הינם מועמדים לכריתת בלוטות לימפה (RPLND). באופן כללי, שלושה מחזורי טיפול כימותרפי בתשלובת BEP מפחיתים את סמני הגידול לערכים תקינים האופיינים ברוב המכריע של החולים23-16.
גידול שארי המתגלה בבדיקות הדמיה הנעשות באופן שגרתי לאחר השלמת הטיפול הכימותרפי, אינו בהכרח מצביע על מחלה פעילה. ב-45 אחוז מהמקרים מדובר ברקמה נמקית בלבד, טרטומה (Teratoma) ב-45 אחוז מהמקרים האחרים, או גידול מסוג שאינו טרטומה (Non-Teratoma) ב-10 אחוז מהמקרים. כריתת בלוטות לימפה אחורי צפקיות, בשילוב או ללא כריתת שאריות גרורות ריאתיות, נדרשת כטיפול להסרה מלאה של המחלה ולשם קביעת ההיסטולוגיה המדוייקת של הגידול. טרטומה אינה רגישה לטיפול כימותרפי ודורשת כריתה לשם השגת ריפוי.
גידול מסוג זה שאינו נכרת, גדל בהדרגה ומוביל להתפתחות תלונות מקומיות כגון כאב או מיימת כלייתית, ואינו נוטה לפיזור גרורתי. במידה ובתוך שארית הגידול נמצאו תאי גידול מהסוגים הבאים: אמבריונאלי, כוריוקרצינומה או קרצינומה ממקור שק החלמון (embryonal, choriocarcinoma or yolk sac carcinoma (אזי יש להמשיך ולטפל בשני מחזורים נוספים בתשלובת הכוללת פלטינול ואתופוסיד (EP). גישה זו המשלבת כימותרפיה וכירורגיה משיגה ריפוי ב-90 אחוז מחולי סרטן אשכים אשר נמצאים בקבוצת סיכון נמוך עד בינוני בשלבי מחלה שני או שלישי.
בחולים עם סיווג פרוגנוסטי מופחת (Poor risk NSGCT), קיים סיכון גבוה להישנות מחלתם והם מתאפיינים ע"י גרורות ויסצרליות שאינן ריאתיות, ערכים גבוהים מאוד של סמנים, או מיקום הגידול הראשוני במיצר. חולים אלו מועמדים לטיפול בארבעה מחזורי טיפול בתשלובת BEP, או לחלופין השתתפות במחקרים. הטיפול הכימותרפי המקובל מקנה כ-50 אחוז סיכוי לריפוי בלבד16,17,24,25.
טיפול קרינתי אינו מיושם באופן שגרתי בגידול מסוג שאינו סמינומה, עם זאת לעיתים נשקל טיפול זה לצורך הקלה של תלונות מקומיות, גרורות מוחיות (לאחר טיפול כימותרפי ראשוני), דחיסת חוט השדרה ((spinal cord compressio, או כאבים גרמיים.
הטיפול בגידול מסוג סמינומה
בגידולים מסוג סימנומה, הגורם הקובע את תוכנית הטיפול הינו שלב המחלה. חולים בשלב קליני ראשון של המחלה לעיתים קרובות נרפאים לחלוטין לאחר התערבות כירורגית של כריתת אשך, אף על פי שיש 15-25 אחוז סיכוי להישנות המחלה באיזור אחורי הצפק. עובדה זו מחייבת מעקב קפדני ביותר לאורך זמן רב. לאור זאת, הטפול המקובל בארה"ב המוצע לאחר כריתת אשך הוא טיפול הקרנתי לבלוטות לימפה הסמוכות לוותין מתחת לסרעפת במנה כוללת של 20-30Gy 16,17,26.
טיפול במחלה בשלב שני (מעורבות בלוטות לימפה אחורי צפקיות בלבד) תלוי בגודל של בלוטות הלימפה הנגועות. טיפול קרינתי הוא טיפול הבחירה בחולים עם בלוטות בקוטר הקטן מ-5 ס"מ. המנה הניתנת היא Gy 35-40, לאיזור בלוטות אחור צפקיות הכוללות לעיתים גם בלוטות מפשעתיות בצד הגידול. מחלה אחור צפקית בעלת נפח גדול עם בלוטות במימדים של 5 ס"מ או יותר, מטופלת ע"י שלושה מחזורים של BEP. טיפול זה מומלץ גם בשלב שלישי של גידול זה בחולים בקבוצת סיכון נמוכה. לחולים בקבוצת סיכון בינוני
(Intermediate risk), כגון עם גרורות ויסצרליות לא ריאתיות, יש לתת 4 מחזורים של BEP 2,16,26,27.
לאחר הטיפול הכימותרפי, במידה וסמני המחלה תקינים, מומלץ לבצע בדיקת CT PET לצורך איבחון רקמה גידולית פעילה. במידה והבדיקה תקינה אין מקום לטיפול נוסף מלבד מעקב. לעומת זאת, במידה והבדיקה חיובית ומצביעה על קליטה מוגברת, יש להמשיך בבירור היסטולוגי וכריתה, או הקרנות לאיזור. לחלופין ניתן לבצע בדיקת טומוגרפיה מחשבית, כאשר במידה ושארית הגידול הינה קטנה מ-3 ס"מ, יש להמשיך במעקב קליני ודימותי. בנושא של הטיפול בממצאים שקוטרם עולה על 3 ס"מ, אין אחידות דעים מאחר וב-25 אחוז מהמקרים יש שיירי גידול פעילים או ממצאים של גידול שאינו סמינומה שלא זוהה בשלב האבחנה. במקרה זה, האפשריות הטיפוליות כוללות: הסרה ניתוחית של הממצא, הקרנות לאיזור או לחלופין המשך מעקב קליני ודימותי2,16.
הטיפול במחלה חוזרת או במחלה עמידה לקו כימותרפי ראשון
סרטן אשכים יחודי בכך שאפילו במקרים של מחלה עמידה לקו ראשון של טיפול כימותרפי, עדיין קיימים אחוזי ריפוי גבוהים. חולים אלו נמנים על שתי קבוצות: הראשונה עם פרוגנוזה טובה ולעומתה קבוצה עם פרוגנוזה פחותה. גורמים המשייכים את החולה לקבוצה פרוגנוסטית טובה כוללים: גידול ראשוני באשכים; הפוגה מלאה של מחלה לאחר קו כימותרפי; רמות נמוכות של סמנים ונפח קטן יחסית של מחלה חוזרת.
טיפול הבחירה בקבוצת חולים אלו הוא 4 מחזורי כימותרפיה בתשלובת ציספלאטין (Cisplatin), איפוספמיד ווינובלסטין ( Ifosfamide Vinblastine), או טקסול ((Taxol (TIP or VIP). במקרים אלו, ב-50 אחוז מהחולים נצפית נסיגה מלאה של המחלה תחת טיפול בתשלובת VIP. כ-25 אחוז משיגים נסיגה מלאה וממושכת במקרה של גידולים מסוג שאינו סמינומה, לעומת 50-60 אחוז במקרים של גידולים מסוג סמינומה. במידה וחולה עמיד לקו טיפול שני הפרוגנוזה עגומה. השתלת מח עצם עצמית, כריתה של גרורה בודדת נגישה או קרינה ממוקמת הן אופציות טיפוליות בשלב זה. טיפול תומך בלבד גם הוא מהווה אפשרות טיפולית סבירה בחולה שכזה28,16.
נזקי הטיפול הכימותרפי
ככימותרפיה בתשלובת BEP עלולה להוביל לדיכוי מח עצם חריף וחום מלווה בנויטרופניה בכ-15 אחוז מהחולים. כימותרפית הצלה מסוג VIP, לדוגמה, עלולה לגרום לחום על רקע נויטרופניה במחצית מהחולים. ציספלאטין עלול לגרום לרעילות מערכת עצבים הקפית מצטברת, רמות נמוכות של מגנזיום ואשלגן בדם (עקב נזק כלייתי-טובולררי), החמרה בתיפקודי כליות, ירידה בשמיעה עקב פגיעה בטונים הגבוהים, וכן טינטון בלתי הפיך. ארבעה מחזורי טיפול בבליאומיצין עלולים לגרום ללייפת (fibrosis) של הריאות. תופעת לוואי זו שכיחה יותר בחולים בגיל מתקדם, קרינה קודמת לבית החזה ותפקוד לקוי של הכליות. אי פוריות בגבר מהווה נושא חשוב בין חולים עם סרטן אשכים המאובחנים בד"כ בשיא גיל הפוריות. חלק משמעותי של החולים מבטא מיעוט זרע כבר באבחון מחלתם ובאחוז משמעותי מהחולים יכולה להחמיר בעיה ראשונית או להתפתח עקרות משנית, לכן, שימור זרע בבנק הזרע טרם התחלת הטיפול הכימותרפי הוא בעל חשיבות מכרעת2.
ד"ר אביבית פאר וד"ר דוד סריד, המערך האונקולוגי, הקריה הרפואית רמב"ם, חיפה