ההתפתחות הטכנולוגית באמצעי הדימות השונים בכלל ובסורק הטומוגרפיה המחשבית (CT) בפרט, אשר באה לידי ביטוי בתוספת שורות של גלאים, הסורקים בו זמנית ומאפשרים קבלת מספר חתכים בכל סיבוב של שפופרת המכשיר (עד 64 שורות גלאים כיום והיד עוד נטויה..) - גרמה למהפכה בתחום הדימות האבחנתי.
הוספת שורות גלאים (והפיכתו של ה-CT מסורק חד פרוסתי לסורק רב פרוסתי) מתבטאת במהירות סריקה גבוהה פי כמה, אשר בתוספת שיפור ביכולת הרזולוציה והעיבוד המחשבי, שיכללה את האבחון הבלתי פולשני של אברי הגוף השונים ברזולוציה גבוהה, בנוסף ליכולת לבצע מספר סריקות חוזרות מהירות בחתכים צפופים. כל אלה, הפכו את הסורק הממוחשב לכלי מרכזי במערך הדימות.
אחד מכיווני ההתפתחות בא לידי ביטוי ביכולת לדמות את כלי הדם העורקיים והוורידיים, שיטה הקרויה CT ANGIOGRAPHY) CTA). טכניקה זו ביטלה, למעשה, את רוב ההתוויות לאנגיוגרפיה קונבנציונלית.
דימות הלב היוותה אתגר, בגלל היות הלב איבר המצוי בתנועה מתמדת. ואם לא די בכך, מדורי הלב, אשר אינם מתכווצים באותו הזמן, ותנועת הנשימה, הפכו את דימות הלב למכשול בדורות הקודמים של הסוקרים. אך לא עוד.
כיצד מתבצע צנתור וירטואלי?
צנתור וירטואלי מתבצע ככל בדיקת CT אחרת עם הזרקת יוד דרך הווריד, בתזמון בו היוד מגיע לעורקים הכליליים. בסורק ה-64 פרוסתי מוזרק יוד בכמות פחותה בהשוואה לבדיקות CT "רגילות"- בדרך כלל די ב-80 סמ"ק יוד, בקצב של 4-7 סמ"ק לשנייה, לצורך דימות העורקים הכליליים בסורק ה-64 פרוסתי.
על מנת לדמות את עורקי הלב ברזולוציה אבחנתית, נדרשת סריקה עם חפיפה בעובי פרוסה תת מילימטרי, תוך עצירת הנשימה וניטור א.ק.ג. המשולב בתוכנת הסריקה. בסורקים הארבע שכבתיים נדרש הנבדק לעצור את נשימתו לכארבעים שניות! בסורק ה-16 פרוסתי קוצרה הסריקה ל- 20 שניות ובסורק ה-64 פרוסתי נדרשת עצירת נשימה לכ-5 שניות בלבד.
על פי רוב, קודמת לסריקה עם חומר הניגוד, סריקה ללא הזרקת חומר ניגוד שמטרתה לכמת את כמות הסידן בעורקים הכליליים (calcium score) בניקוד לפי אגטסטון (המחושב לפי מכפלת שטח ההסתיידות במילימטר רבוע), שמצא יחס ישר בין ניקוד הסידן לבין קיום מחלה טרשתית בעורקים הכליליים.
הסידן בעורקים הכליליים גורם לארטיפקט מהיותו בעל צפיפות גבוהה מהיוד המוזרק. הארטיפקט הקרוי blooming effect, גורם לסידן להיראות גדול יותר מגודלו האמיתי, ומקשה על דיוק קביעת קוטר העורק בסמוך לסידן. בעיה זו חמורה בעיקר בסורקים מהדורות הקודמים. במספר מקומות נקבע רף מרבי לכמות הסידן המומלצת להמשך הבדיקה עם הזרקת חומר ניגודי, על מנת לשמור על רגישות גבוהה.
רווח משני נוסף המתקבל מהסקירה ללא הזרקת חומר הניגוד הינו הדגמת כל בית החזה, המאפשרת בדיקת שדות הריאה לזיהוי מוקדם של סרטן הריאה או פתולוגיות אחרות במיצר, בצוואר וברום הכבד, הטחול, רום הכליות, השלד הגרמי ובבלוטות יותרת הכליות. בכמה עבודות נמצא שיעור ממצאים חוץ כליליים גבוה יותר משיעור הממצאים הכליליים - בעיקר מוקדים ריאתיים.
קיימות שתי שיטות לאיסוף נתונים מהסריקה. בראשונה, נקבע זמן שרירותי בתוך מחזור הלב ובסריקה דוגמים את הלב רק באותו הזמן (prospective gating). בשיטה השנייה, מתבצע איסוף נתונים כמעט רציף המאפשר ניתוח רטרוספקטיבי של עורקי ומדורי הלב בכל חלק (פאזה) של מחזור הלב
(reterospective gating).
נמצא, כי איכות הסריקה עולה ככל שקצב הלב יורד ולמרות שניתן להדגים את העורקים הכליליים גם בקצב של 80 פעימות לדקה ויותר, סריקה בקצב לב נמוך מ-60 היא אידיאלית. לצורך כך, לאחר תרגול תוך ניטור א.ק.ג לקביעת קצב הלב תוך עצירת נשימה, מקבלים רוב הנבדקים תרופה להאטת הקצב, בדרך כלל חוסמי ביטא. במקרים בהם קצב הלב אינו סדיר, לא ניתן לדגום את העורקים בדיוק באותו שלב במחזור הפעימות, לכן נבדקים עם קצב לב לא סדיר אינם מתאימים לבדיקה. עם זאת, בחלק מהסורקים, במידה ומופיעה פעימה אחת אקטופית, ניתן להסירה ולבצע את בניית התמונה ללא הדגימה מהפעימה האקטופית.
במקרים בהם נבדקים אנשים שעברו ניתוח מעקפים, מורחב שדה הבדיקה ונכללים העורקים התת בריחיים ודופן בית החזה בסריקה, לשם הדגמת כל מגוון המעקפים.
עיבוד הנתונים
הנתונים הגולמיים מתקבלים כחתכים אקסיאלים רציפים של כל הלב ב- 10 שלבים (פאזות) בתוך מחזור פעימת הלב. בכל סריקה מתקבלים למעלה מ-200 חתכים, כך שבדיקת הלב מכילה למעלה מ-2,000 חתכים.
על פי רוב, די בסריקה של השליש השלישי של הדיאסטולה, אז הלב נע במידה הפחותה ביותר, אולם לפעמים יש צורך בעיבוד פאזות נוספות.
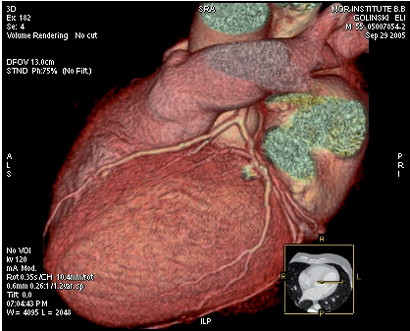
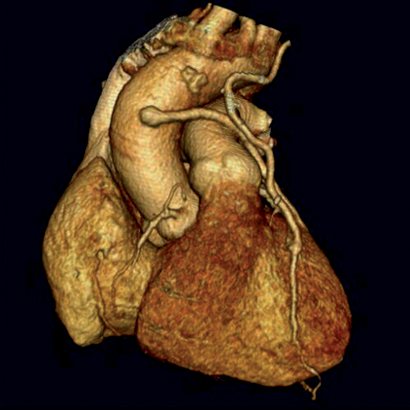
באמצעות תכנות מחשב, ניתן להסב את המידע האקסיאלי לתצוגה דו או תלת ממדית: ניתן ליישר ולפרוס את העורק לאורך צירו ולסובבו סביב הציר כאוות נפשו של המפענח, לצורך הערכה של מידת ההיצרות בכל כיוון. ניתן להדגים את העורקים הכליליים יחד עם הלב בתמונה תלת מימדית הניתנת לסיבוב בכל ציר (volume rendering) (ראה תמונה מס' 1) או את העץ הכלילי לבד
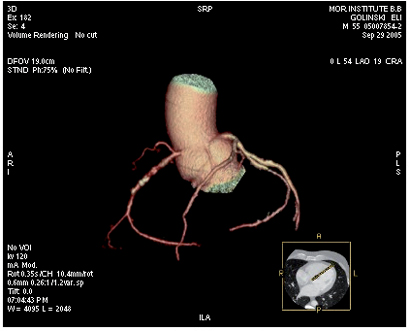
(tree) (ראה תמונה מס' 2).
תמונה מס' 1 :תמונת volume rendering של הלב מלפנים. מודגם עורק כלילי ראשי (left main artery )העורק השמאלי הקדמי היורד , חלק מהעורק הסובב השמאלי (cx)והענף המרגינלי הראשון.
תמונה 2 :תמונת volume rendering של עץ העורקים הכליליים באותו נבדק :מודגמים רבדים מסויידים לאורך החלק הקריבני של העורק הכלילי הימני
ניתן לעגל את הלב לצורת כדור בכדי להקל על הצפייה (globe view) ולשוטט בתוך חלל העורקים ( virtual endoscopy), ועוד.
הקפאת תנועת הלב ודגימה באותו מקום ובאותה פאזה, מאפשרת הקטנת הארטיפקטים למינימום וזיהוי פתולוגיות בדפנות העורקים לכדי אבחנה בין רובד טרשתי מסויד, רובד פיברוטי, רובד שומני, ורובד מעורב (תמונות 3-6) (באמצעות מדידת הצפיפות ביחידות האונספילד).
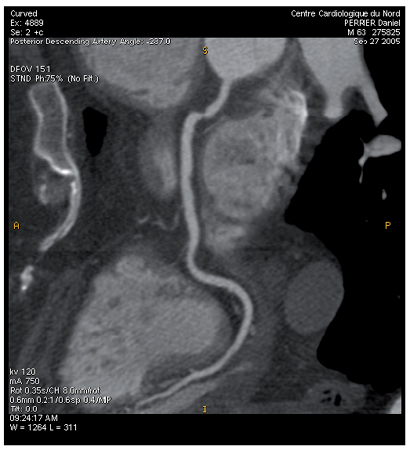
תמונה 3 :תמונה דו-מימדית של העורק הכלילי הימני, המדגים היצרות בינונית קצרה בחלקו הקריבני.
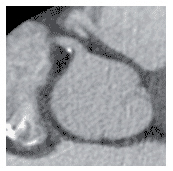
תמונה 4 :רובד טרשתי מעורב ,בדרגת היצרותקלה במוצא העורק הכלילי הימני. המוקד הלבן הינו סידן והשחור שומן
תמונה 5 :תמונה דו מימדית מיושרת של העורק הסובב השמאלי.מודגמת חסימה ממוצאו עם חידוש זרימה בהמשכו.מימין מודגמים חתכים אקסיאלים בציר העורק באזור החסימה , המראים חוסר האדרה של העורק באזור החסום
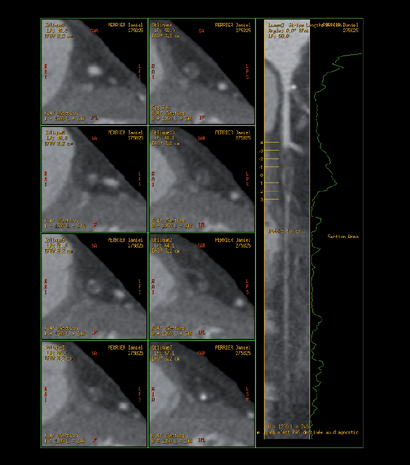
תמונה 6 א' : היצרות בשיעור 70%-50% בחלק הקריבני של העורק הכלילי הקדמי היורד (LAD )בשחזור דו מימדי
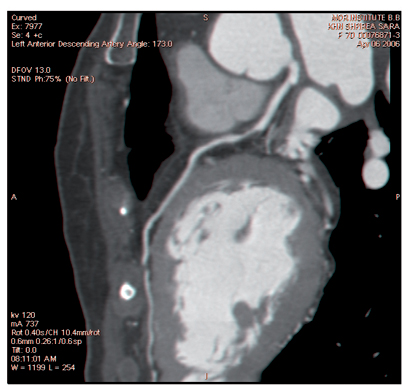
תמונה 6 ב':ממצא זהה בצנתור
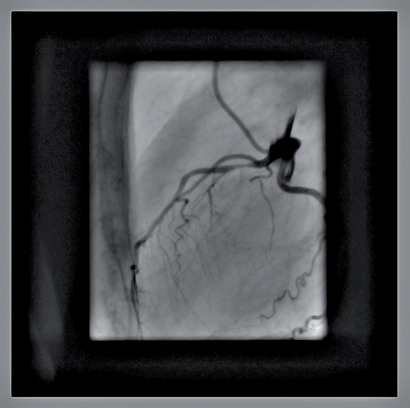
בניגוד לצנתור, בו מודגם רק החלל (לומנוגרפיה) ואין יכולת לראות מה "מתחבא" מעבר להיצרות אלא אם משתמשים ב-IVUS, ניתן לראות positive remodeling, קרי, גדילת העורק ללא שינוי בקוטרו הפנימי - ממצא שלעיתים לא ניתן לזהותו בצנתור - או negative remodeling, שמשמעותו הקטנת קוטר הכלי ללא רובד טרשתי פנימי.
ניתן לזהות בבירור אוטמים של כל עובי השריר או חלקו (תת אנדוקרדיאלי) ודלף בין עלייתי או בין חדרי, לבצע חישובים של ejection fraction ,cardiac output לדמות תנועה ולחשב שטח מסתמים, טבעיים ומלאכותיים, ללא צורך בביצוע סריקות נוספות.
בגלל כמות הנתונים הרבה והצורך לזהות כל עורק בנפרד, לפעמים בכמה פאזות, נדרשת מיומנות גבוהה של הרדיולוג המפענח. בממוצע, משך העיבוד והניתוח של בדיקה "רגילה" בסורק ה-64 פרוסתי אורך כחצי שעה.
רגישות, סגוליות ומגבלות הבדיקה
רגישות וסגוליות דימות העורקים הכליליים על ידי סורק, גבוהה. רגישות הבדיקה נעה סביב 95% והסגוליות סביב 98% בזיהוי היצרויות, מעל 50% וקרוב ל-100% בניבוי negative predictive value. ערכים אלו גבוהים מרגישות וסגוליות מבחן מאמץ, ממיפוי הלב, ומבדיקת העורקים הכליליים באמצעות תהודה מגנטית.
מהלך של העורק הכלילי בתוך שריר הלב (intramyocardial bridge) הינו ממצא שכיח שמשמעותו אינה ברורה, המצוי בכ-18% מכלל האוכלוסיה. הוא ניתן לזיהוי בקלות ע"י CT אולם קשה לזיהוי בצנתור.
הבדיקה אינה מושלמת וכוללת כמה חסרונות. ראשית, יש שימוש בקרינת רנטגן, ברמה הגבוהה מכמות הקרינה שהנבדק סופג בבדיקות CT אחרות. רמה זו שווה לקרינה הנצברת במיפוי טכנציום, נמוכה פי 3 מהקרינה הכרוכה במיפוי תליום(!) וגבוהה במקצת מהקרינה הממוצעת בצנתור לב.
הבדיקה צורכת שימוש ביוד על סכנותיו ומגרעותיו, אם כי בכמות פחותה מ-CT רגיל ושווה לצנתור ממוצע. רמת סידן גבוהה בעורקים הכליליים מורידה את רמת דיוק הבדיקה, וכמובן שנדרש שיתוף פעולה מהנבדק בעצירת נשימה וחוסר תזוזה בעת הסריקה.
מי מתאים לבדיקה?
טרשת העורקים הכלילית הינה הגורם הראשון לתמותה בגברים ובנשים בעולם המערבי ובישראל. תסמונת כלילית חריפה (acute coronary syndrome) מאובחנת בישראל בלמעלה מ-30,000 איש בשנה, וכ-45% מהלוקים בתסמונת עלולים למות בתוך שעה מהופעת הסימנים. זיהוי מוקדם של טרשת עורקים בעורקים הכליליים וטיבם של הרבדים, יאפשר טיפול מונע במחלה ונסיגה שלה.
בדיקת הזיהוי המדויקת ביותר בספרות הינה צנתור, על מגבלותיו והסכנות הגלומות בו. במדינת ישראל מתבצעים למעלה מ- 40,000 צנתורים של עורקי הלב בשנה, כמחציתם אבחוניים בלבד. השיטות הלא פולשניות כוללות מבחן מאמץ ומיפוי על סוגיו השונים. לשתי הבדיקות רגישות וסגוליות מוגבלים והמיפוי כולל שימוש בחומר רדיואקטיבי.
כיוון שמדובר בבדיקה עם קרינת רנטגן, אין הבדיקה מומלצת כבדיקת סקר לכל האוכלוסיה הצעירה ולאנשים עם רגישות ליוד או עם אי ספיקת כליות, אלא לאנשים אסימפטומטים עם גורמי סיכון להופעת מחלת לב טרשתית, אנשים סימפטומטים שהצנתור בהם קשה או אינו אפשרי ובנבדקים לאחר ניתוח מעקפים או השתלת תומכן - שכן אין בעיה בסורקים החדשים לדמות עורקים עם תומכנים (סטנטים) (ראה תמונה מס' 7) ולזהות היצרויות או חסימות בתוך או בצמוד לתומכנים. אין מגבלה לסריקה בדימות מעקפים, שהינה בדיקה קשה וממושכת בצנתור, שכן בסריקה אחת מודגם כל האזור (ראה תמונה מס' 8).
תמונה 7 : מצב לאחר השתלת 4 תומכנים בעורק הכלילי הימני -היצרות קלה של 50% ביציאה מהתומכן הרחוק
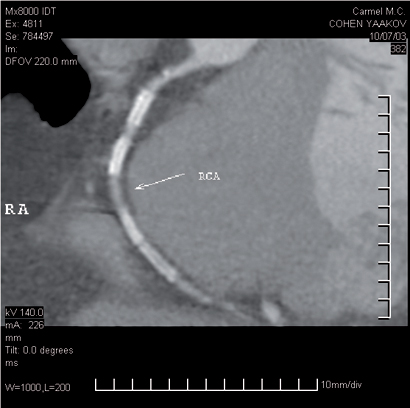
תמונה 8 :מצב לאחר CABG. מעקף LIMA ל-LAD עם חיבור פתוח להמשך ה- LAD ומעקף וורידי מהוותין לעורק ההיקפי השמאלי.החיבור לעורק לא מודגם במישור זה וכן מוצא ה-LIMA , שהודגמו במנחים אחרים
במספר בתי חולים משתלב הסורק בעיבוד נתוני חולים עם כאבים בחזה ללא ממצאים תומכים בא.ק.ג, או בבדיקות המעבדה, ומאפשר זיהוי או שלילת הסיבות להופעת התסמינים של מחלה כלילית חדה, דיסקציה אאורטלית, תסחיף ריאתי, דלקת ריאות לא טיפוסית ועוד - והכול בסריקה אחת.
בעבודות שסקרו נבדקים אתסמיניים עם גורמי סיכון נמצא שיעור ממצאים כליליים בדרגות שונות של כ-50%, מתוכם הופנו לצנתור או לניתוח מעקפים בשל קיום מחלה כלילית קשה כ-4%!
שיפורים נוספים במספר שורות הגלאים (כיום עובדים על פיתוח 256 שורות, שמשמעותו דגימת פעימה אחת בלבד!), ובצורת הסריקה בה כמות הקרינה לא תהא אחידה אלא ממוקדת לשלב קצר אחד, כך שתפחית את כמות הקרינה ב 70% לפחות, תשפר יותר את דיוק הסריקה ותאפשר שימוש נרחב יותר עם התוויות רחבות יותר לבדיקה.
ד"ר אלי עטר, מנהל המערך לרדיולוגיה פולשנית, המרכז הרפואי רבין, קמפוס גולדה, פתח תקוה