מערכת חיסון תקינה מגינה על גופנו מרוב גורמי המחלות הזיהומיות, ע"י שימוש משולב בכל מרכיביה- הגנה על משטחים (עור וריריות), תאים (לימפוציטים, גרנולוציטים, מאקרופאגים וכו') וגורמים מומסים (נוגדנים, חלבוני המשלים, ציטוקינים וכו'). מצב גופני טוב, מצב תזונתי אופטימלי, כיסוי עור וריריות יעיל ותפקוד איברים תקין, ביחד עם תפקוד תקין של מרכיבי החיסון התאי וההומורלי, מספקים הגנה כנגד מרבית המיקרואורגניזמים (חיידקים, וירוסים, פטריות וטפילים). גם לאוכלוסיית החיידקים המצפה את גופינו, יש תפקיד חשוב בהגנה עליו, ע"י תחרות עם חיידקים אלימים יותר, על אתרי קשירה ומזון.
כל חולה שבו אחד או יותר ממנגנוני החיסון לקוי, סובל מדיכוי חיסוני.
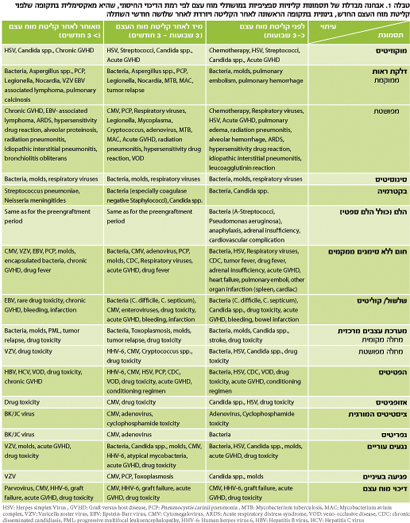
הסיכון לזיהומים תלוי בעומק הדיכוי החיסוני. דיכוי חיסוני מקסימלי נצפה בתקופה הראשונה לאחר השתלות ממוח עצם, כאשר מערכת החיסון של החולה נהרסת ע"י טיפול כימותרפי מסיבי, ומערכת החיסון המושתלת טרם נקלטה. בהמשך, רמת החיסון עולה עם הזמן, עד לשלב בו אינו זקוק לתרופות והדיכוי החיסוני הוא מזערי. לעומת זאת, מושתלי איברים יקבלו תרופות כנגד דחייה כל תקופת ההשתלה והם יישארו מדוכאי חיסון ברמה התלויה בסוג ובכמות התרופות.
כמות המטופלים בטיפול מדכא חיסון בגלל השתלות איברים, השתלות מוח עצם, גידולים ממאירים המטולוגיים וסולידיים ומחלות דלקתיות אוטואימוניות, גדלה בהתמדה מאז השתלת הכליה הראשונה שנעשתה ב-1954. הדיכוי החיסוני יכול להיות קצר (כימותרפיה), מס' חודשים (השתלות מוח עצם) או קבוע (השתלות איברים, אימונוסופרסיה).
זיהומים הם גורם התחלואה והתמותה העיקרי בחולים מדוכאי חיסון. כדי לאפשר טיפול במחלה הגורמת לדיכוי החיסוני (כגון ממאירות המטולוגית), או לאפשר טיפול שבעצמו גורר דיכוי חיסוני (כגון טיפול כימותרפי), צריך להציע לחולה הגנה טיפולית מיטבית כנגד הזיהומים שהוא עלול לפתח. כתוצאה מגידול האוכלוסיה מדוכאת החיסון, הנגזר מאיכות ואורך החיים המשתפרים כל הזמן, מתגלים זיהומים אופורטוניסטים חדשים לבקרים. יש צורך במעקב צמוד, צפיית הסיבוכים מראש, וטיפול בתחילת כל זיהום.
עקרונות האבחון והטיפול בזיהומים במדוכאי חיסון
- גורמי הזיהומים בחולים אלו מגוונים וכוללים מיקרואורגניזמים הגורמים לזיהומים גם באוכלוסיה הבריאה ובנוסף מיקרואורגניזמים הגורמים זיהומים אופורטוניסטים. כך, שדלקת ריאה בחולים אילו יכולה להגרם מהחיידקים השכיחים בקהילה (Streptococcus pneumoniae ,Haemophilus influenzae, Moraxella catarrhalis, Mycoplasma pneumoniae, Chlamydia) או כתוצאה ממיקרואורגניזמים אופורטוניסטים הפוגעים רק במדוכאי חיסון כמו:
Pneumocystis jirovecii, Nocardia, Rodococcus equi, Legionella, Aspergillus, Cryptococcus neoformans, CMV, VZV,Respiratory sincytial virus) RSV).
- התגובה הדלקתית הנגרמת בעקבות חדירת מיקרואורגניזמים לגוף, פגועה בחולים מדוכאי חיסון. לכן, הסימנים הקליניים הקשורים למחלה
הם לעיתים דלים ולא אופיינים וכך גם הסימניםהרנטגניים. זו הסיבה לכך שפעמים רבות, החולה מאובחן רק כאשר המחלה כבר מפושטת.
- יצירת נוגדנים והיפוך סרולוגי (Seroconversion) בחולים מדוכאי חיסון הם איטיים מהרגיל.לכן, בדיקות סרולוגיות אינן אבחנתיות למחלה
חריפה ויש להשתמש בבדיקות לגילוי המזהם עצמו (תרביות), או לגילוי אנטיגן שלו(IF, ELISA), או שימוש בשיטות מולקולריות לגילוי מזהם ספציפי מהדם או מרקמה נגועה כגון PCR ((Polymerase chain reaction.
- שינויים אנטומיים לאחר ניתוחי השתלה, משנים את הסימנים הקליניים במושתלי איברים.לעיתים קרובות, דרושות בדיקות הדמייה כמו
CT ו-MRI כדי לראות עדות לתהליך זיהומי באיבר המושתל או סביבו.
- לאבחנה מיקרוביולוגית ספציפית יש צורך לעיתים לבצע ביופסיות לבדיקות היסטופאתולוגיות ומיקרוביולוגיות. יש לבצע את הבדיקות בתחילת המחלה, לפני שהמחלה מתקדמת ואין אפשרות לבצע פרוצדורות מסוג זה. בדיקות אילו משפרות את הסיכוי לאבחנה נכונה וטיפול מוצלח, ומקטינות את הסיכון שבטיפול רחב טווח.
- יש לקחת בחשבון תגובות צולבות בין התרופות הרבות שהחולה מקבל, ריבוי התרופות האנטי-מיקרוביאליות וכל תופעות הלוואי שלהן.
- בבחירת הטיפול יש לקחת בחשבון שיציבות של מיקרואורגניזמים לאנטיביוטיקה עולה בשנים האחרונות, בעיקר בחולים הקשורים למערכת הבריאות (אשפוז בבתי חולים, ביקור במרפאות לעיתים קרובות), דוגמת החולים מדוכאי החיסון.
- לעיתים, יש לשלב כירורגיה בטיפול בזיהומים (הטרייה), כיוון שטיפול אנטיביוטי בלבד אינו מספיק.
- לפעמים, יש צורך להפסיק את הדיכוי החיסוני על מנת לאפשר ריפוי מהמחלה הזיהומית (ולהציל את חיי החולה). טיפול זה עלול להחמיר את המחלה היסודית, להגביר דחיית שתל או אף להביא לאיבוד האיבר המושתל.
טיפול מונע
מכל הסיבות שהובאו לעיל, ברור שבמדוכאי חיסון קשה לטפל בזיהומים ויש להתרכז במניעתם. הטיפול המונע מותאם לחולה ולרמת הדיכוי החיסוני שלו וכולל: הכנת חולה ע"י אבחון וטיפול במחלות זיהומיות לפני השריית הדיכוי החיסוני (דוגמת טיפולי שיניים, שחפת, טפילים) - (לא תמיד אפשרי).
- מתן חיסונים לפני השריית הדיכוי החיסוני. לעתים, במיוחד לפני השתלת אברים סולידיים החיסוניות טובה יותר וניתן לחסן אף בחיסונים חיים מוחלשים ולהשלים חיסונים אחרים.
- לאחר השריית הדיכוי החיסוני יש לתת בצורה קבועה חיסונים מומתים או מרכיבים של הפתוגן בלבד, כנגד מחלות זיהומיות שונות (שפעת, פנוימוקוק וכו')או מעקב צמוד אחרי פרוטוקול חיסונים מתאים למחלה.
- הדרכה למניעת חשיפה לזיהומים בזמן אשפוז (רחיצה וחיטוי, שימוש במסכה, בידוד לפי הצורך).
- הדרכה למניעת חשיפה לזיהומים בקהילה (מניעת מגע עם חולים במחלות זיהומיות מדבקות, מניעת מחלות המועברות ע"י בעלי חיים, וכד').
- מתן טיפול אנטיביוטי מונע, לפי פרוטוקולים מקובלים לרמת הדיכוי החיסוני (כנגד PCP או CMV או HSV).
- מתן טיפול אנטיביוטי מונע או טיפול בנוגדנים ספציפיים למחלה זיהומית, אליה נחשף מדוכא החיסון, במטרה למנוע התפרצות קלינית (דוגמת שחפת, אבעבועות רוח, חצבת ועוד).
- מתן טיפול אנטימיקרוביאלי סופרסיבי לחולה שעבר התפרצות של מחלה זיהומית רדומה בזמן הדיכוי החיסוני, כל זמן שהוא נמשך (כמו טיפול כנגד HSV, VZV).
זיהומים בחיידקים
בתקופה של דיכוי חיסוני עמוק או בתקופה המידית לאחר השתלה
(טבלה 1), חיידקים אירוביים גרם חיוביים או גרם שליליים הם גורמי הזיהומים. בשלב זה יש נזק לעור (נגעים, עירויים) ולריריות (מוקוזיטיס) עקב הטיפול, וכן נויטרופניה קשה. מקורות חדירה אפשריים כוללים את העור דרכו חודרים חיידקים כמו Coagulase negative Staphylococcus או Staphylococcus aureus או .Streptococci המעי הפגוע הוא מקור לחיידקים גרם שליליים כמו Enterobacteriaceae, Pseudomonas aeruginosa Stenotrophomonas, maltophilia ועוד. אתרי הזיהום השכיחים הם דם, ריאות ומערכת העיכול (neutropenic enterocolitis).
שלשול שכיח בזמן מוקוזיטיס קשה בגלל הנזק המקומי לרירית המעי, כתוצאה מטיפול או מ-Acute graft versus host disease) GVHD), בשל רגישות לתרופות וגם בגלל זיהומים. הזיהום השכיח ביותר הוא Clostridium difficile associated diarrhea, אך גם מזהמים אחרים יכולים לגרום לשלשול (חיידקים, וירוסים, פטריות, טפילים ומיקובקטריות), בשלבים של דיכוי חיסוני ממושך יותר.
חולים עם דיכוי חיסוני ממושך כתוצאה מדיכוי הומורלי ותאי, ירידה ברמת הנוגדנים, הפרעה באופסוניציה ובפעילות מאקרופאגים, או במצב לאחר כריתת טחול, סובלים מזיהומים, הנגרמים ע"י חיידקים עם קפסולה כמו Streptococcus pneumoniae, Haemophilus influenzae, Neisseria meningitides. בחולים עם מחלת חום ונויטרופניה יש להתחיל מידית בטיפול אנטיביוטי אמפירי המקטין את התמותה. הטיפול כולל שילוב של אנטיביוטיקות, אם כי ניתן להשתמש גם באנטיביוטיקה רחבת טווח בודדת. על מנת להוריד שכיחות זיהומים אילו יש הממליצים לתת טיפול אנטיביוטי מניעתי בפלואורוקינולונים בתקופת דיכוי חיסוני עמוק.
זיהומים במיקובקטריה
זיהומים אלה נחלקים להתלקחות שחפת הנגרמת ע"י Mycobacterium tuberculosis ומחלות הנגרמות ע"י atypical mycobacteria. מומלץ לבדוק כל מועמד לטיפול מדכא חיסון ע"י תבחין PPD וצילום חזה, לגילוי שחפת ישנה, פעילה או רדומה ולטפל בה.
זיהומים בפטריות
הסיכון לזיהום פטרייתי עולה ככל שעולה רמת הדיכוי החיסוני ולכן הסיכון גבוה לאחר השתלת אברים. נהוג לחלק את הפטריות לפי המבנה שלהן והמחלות שהן גורמות לשמרים (yeast) ועובשים (Molds).
זיהום בשמרים (Candidiasis)
גורמי סיכון לזיהום פולשני בקנדידה הם נויטרופניה עמוקה וממושכת, שימוש באנטיביוטיקה רחבת טווח, נזק לריריות, אי ספיקת איברים וקולוניזצית קנדידה באתרים שונים בגוף. זיהום בקנדידה יכול להיות מקומי (עור וריריות) או מפושט כולל אלח דם וזריעה של איברים כמו כבד וטחול. פריחה מאקולופפולריות יכולה להוות עדות ראשונה לקנדידיאזיס מפושטת.
בחולים עם דיכוי חיסוני עמוק מקובל לתת טיפול מונע באזול (Fluconazole). טיפול זה הפחית משמעותית את התחלואה והתמותה מקנדידיאזיס, אך גם העלה את שכיחות הזיהומים מקנדידות עמידות לתרופה זו כמו C. krusei, C. glabrata.
חולים נויטרופנים שאינם מטופלים בטיפול מונע אנטי-פטרייתי ומפתחים חום ועלייה בתפקודי כבד, חשודים לקנדידיאזיס מפושטת עם תסחיפים ספטיים בכבד ובטחול (hepaosplenic candidiasis).
זיהום בעובשים
זיהומים בעובשים כגון Aspergillus, Fusarium, zygomycetes אופיינים לדיכוי עמוק חריף או ממושך של מערכת החיסון, כמו לאחר השתלת מוח עצם עם קליטה מאוחרת של השתל, טיפול לדחיית השתל וזיהום בו זמנית
ב-CMV. זיהום בעובשים מתפתח בעקר בריאות, בסינוסים במערכת העצבים המרכזית ובעור. בשל העלייה בשימוש בווריקונזול לזיהום באספרגילוס, חלה לאחרונה עלייה בשכיחות זיהומים הנגרמים על ידי עובשים עמידים לווריקונזול, כמו משפחת הזיגומיצטים.
Pneumocystis carinii pneumonia) PCP)
זיהום ב-Pneumocystis jerovicii מתפתח בחולים העוברים השתלות אברים, אלו המטופלים בטיפול כמותרפי וסטרואידים. פתוגן זה שהיה מקובל כפרוטוזואה, לאחרונה הוגדר כפטריה. המחלה מתבטאת בדלקת ריאות אינטרציציאלית סוערת. בחולים עם דיכוי רציני של מערכת החיסון מקובל לתת טיפול מונע ב-Trimethoprim/ Sulfamethoxazole.
זיהומים נגיפיים
אותם נגיפים הגורמים למחלה קלה וחולפת באנשים עם מערכת חיסון תקינה, עלולים להיות קטלניים בחולים עם מערכת חיסון מדוכאת, בעיקר דיכוי בחיסון התאי.
נגיפים ממשפחת ההרפס (CMV, EBV, HSV, VZV, HHV6, HHV7, HHV8) עלולים להתלקח, ובניגוד לאנשים עם מערכת חיסון תקינה בה ההתלקחות חסרת תסמינים, בחולה עם דיכוי חיסוני הם עלולים לגרום למחלה חוזרת וקשה. זיהום עם נגיפים אילו גורם להחמרת הדיכוי החיסוני.
Herpes simplex virus) HSV)
באנשים עם מערכת חיסון תקינה HSV גורם ל-Herpes labialis הנגרם בעיקר ע"י HSV type I ו-Herpes genitalis הנגרם בעיקר ע"י HSV type ואנצפליטיס.
בחולים מדוכאי חיסון, המודבקים בנגיפים אלו, נצפות התפרצויות תכופות המתבטאות בנגעים רבים ורגישים יותר, לתקופות ארוכות. לכן, מקובל לתת טיפול מונע ב- Acyclovir בחודשים הראשונים לאחר השתלות.
Cytomegalovirus) CMV)
באנשים עם מערכת חיסון תקינה, CMV גורם למחלת חום, הגדלת בלוטות, והפרעה בתפקודי הכבד. ההחלמה עצמונית. בחולים מדוכאי חיסון המחלה נגרמת לא מזיהום ראשוני כמו באנשים בריאים, אלא מהתלקחות הנגיף. הביטוי הקליני שונה וכולל מחלת חום, פנוימוניטיס, אנטריטיס, הפטיטיס, רטיניטיס, אנצפליטיס ודיכוי מוח עצם. במושתלי איברים הפגיעה העיקרית היא באיבר המושתל (כליה, כבד, ריאה וכד'). הדיכוי החיסוני שגורם הנגיף מגביר זיהומים משניים בחיידקים ופטריות.
הסיכון לפתח מחלת CMV עולה בחולה סרו-שלילי המקבל שתל מתורם
סרו-חיובי, בחולים בהם נמדדת רמת נגיף גבוהה בדם, כשהשתל עם רמת התאמה לא מירבית, גיל מבוגר, כשניתן טיפול מקדים להשתלה בהקרנה כל גופית (TBI), או טיפול בשתל מוח עצם מנוקה מלימפוציטים T עם CD34 וב-GVHD חריף. מקובל היום למנוע מחלת CMV בתקופה הראשונה שלאחר השתלה (3 חודשים לפחות ע"י טיפול מונע ב-Ganciclovir) GCV ) או Valgancyclovir או ע"י טיפול מקדים, בעזרת מעקב שבועי אחרי רמת הנגיף בדם ומתן טיפול בעליית הרמה, עוד טרם יתגלו סימנים קליניים במטופל (Preemptive therapy).
Human Herpesviruses 6,7,8) HHV6,7,8)
התלקחות של HHV6 נצפית ב-40-60 אחוז ממושתלי מוח עצם כשלושה שבועות אחרי השתלה, אך המשמעות הקלינית של תופעה זו לא ברורה. במיעוט החולים המחלה עלולה להתבטא בפריחה, חום, דלקת ריאות אינטרסטיציאלית, אנצפליטיס או דיכוי מוח עצם. טיפול בנוגדנים מונוקלונליים כנגד CD3 ו-GVHD מעלים את הסיכון להתלקחות והתפרצות אנצפליטיס. מכיוון שזיהום זה גורר דיכוי חיסוני בעצמו, הוא חושף את החולה לזיהומים נגיפיים אחרים כמו CMV או EBV.
התלקחות של HHV7 בתקופה הראשונה לאחר השתלת מוח עצם, קשורה כנראה לקליטת שתל ארוכה מהרגיל, אך תפקידו אינו ברור.
התלקחות או הדבקה חדשה ב-HHV8 נצפתה בחולים לאחר השתלת מוח עצם אך המשמעות הקלינית אינה ברורה.
Epstein-Barr virus) EBV)
התלקחות EBV במדוכאי חיסון שכיחה, אך תחלואה נלוית נדירה ונצפית בזמן דיכוי חיסוני ניכר. ספקטרום הזיהום כולל עלייה בהפרשת הנגיף בדרכי הנשימה העליונות ללא תסמינים, תסמונת לא ספציפית עם חום ונויטרופניה, Oral hairy leukoplakia, אנמיה אפלסטית, מנינגואנצפלטיס, ו-PTLD Post Transplantation Lymphoproliferative Disorder.
PTLD יכול להופיע כמחלה קלה עד סוערת המתבטאת במחלה נודולרית מקומית עד להתפתחות לימפומה מפושטת. בתחילת המחלה, יכולה להופיע תסמונת דמויית מונונוקלאוזיס אך בהמשך תתכן מעורבות של מערכת העיכול
(25 אחוז), עם סיכון מוגבר לדמם והתכייבות, מעורבות מערכת עצבים מרכזית
(10 אחוז) או מחלת בלוטות עם לחץ מקומי. PTLD נובע מפרוליפרציה של תאי B פוליקלונליים או מונוקלונליים, בדר"כ ממקור התורם, כתוצאה מכשלון חיסוני של תאי T מחוסנים כנגד EBV בחולה. שכיחות המחלה עולה עם קבלת שתל ללא התאמה מירבית, שתל שהוצאו ממנו תאי T, טיפול מדכא חיסון ב-antithymocyte globulin) ATG) או נוגדנים מונוקלונליים כנגד תאי T (הניתנים למניעת דחיית השתל ו-GVHD). אבחנה נעשית על ידי מעקב אחרי רמות הנגיף בדם או ביופסיה מבלוטות נגועות. הטיפול כולל מלבד אציקלוויר, הפסקת/ הפחתת הדיכוי החיסוני במידת האפשר ו/או טיפול מקובל כנגד לימפומה.
Varicella zoster virus) VZV)
התלקחות של VZV שכיחה במושתלי מוח עצם ואיברים וגם במדוכאי חיסון אחרים. הזיהום יכול להתבטא בפריחה שלפוחיתית לאורך דרמטום (שלבקת חוגרת), אך גם להתפשט ולגרום למחלה סיסטמית מסכנת חיים בעיקר במושתלי מוח עצם בשנה הראשונה לאחר ההשתלה. הסיבוכים הידועים כוללים התפשטות עורית של המחלה, כאבים ((neuralgia פוסט-הרפטים, צלקות, זיהום בקטריאלי משני, מעורבות מערכת העצבים המרכזית ואפילו מוות.
במדוכאי חיסון זיהום ב-VZV ארוך יותר עם הבראה איטית. גורמי סיכון להתפרצות VZV כוללים אירוע קודם טרם השתלה, טיפול מונע דחייה מוגבר
(TBI, ATG) וממאירות המטולוגית. סיכון מוגבר להתפשטות המחלה נצפה בזמן טיפול כנגד GVHD חריף, בנוכחות ירידה חמורה בספירת לימפוציטים. טיפול מונע ב-Acyclovir לאחר השתלת מוח עצם מוריד את הסיכון לתחלואה בשנה הראשונה לאחר השתלה. בזמן התפרצות המחלה הטיפול במינון גבוה של Acyclovir ונגזרותיו הינו יעיל.
Adenovirus
העברת נגיף אדנו מאדם לאדם נעשית ע"י זיהום נשימתי טיפתי או מעבר פקאלי-אורלי. הסיכון למחלה סוערת הוא בעיקר בחולים עם GVHD לאחר השתלת מוח עצם. הנגיף עלול לגרום לפנאומוניטיס, נפריטיס, קוליטיס וציסטיטיס המורגיים. תוארה גם נשאות חסרת תסמינים בדרכי נשימה עליונים.
Respiratory viruses
Respiratory syncytial virus (RSV),Influenza, parainfluenza, Rhinovirus, human metapneumovirus - כולם יכולים לגרום למחלה קשה של מערכת הנשימה במדוכאי חיסון. חומרת המחלה תלויה בעומק הדיכוי החיסוני.
נגיפים אחרים
לאחר השתלת מוח עצם, מאבד המושתל את הזיכרון החיסוני ולכן חשוף למחלות כמו חצבת, חזרת, אדמת, זיהום ב-Parvovirus B19, נגיפי BK/JC.
הביטוי הקליני יכול להיות אנמיה קשה בזיהום עם Parvovirus B19, ציסטיטיס המורגית ממושכת בזיהום עם נגיף ה-BK, או לאוקואנצפלופתיה מולטיפוקאלית מתקדמת (PML) עם נגיף ה-JC.
התלקחות של Hepatitis B virus) HBV) ו/או Hepatitis C virus) HCV) לאחר השתלות שכיחה, ובמושתלי כבד עלולה לגרום לנזק מצטבר לשתל, בדומה למחלה היסודית עד להתפתחות צירוזיס חוזרת כבר שנה לאחר ההשתלה. בחולים עם HBV נהוג לפיכך לטפל מניעתית בנסיוב היפראימוני
(HBIG) וב-.lamivudine
זיהומים בטפילים
הזיהום הנפוץ בארצות מפותחות בטפילים הוא Toxoplasmosis. באזורים אנדמיים, יש סיכון להדבקה והתפתחות זיהום ב-Strongyloidiasis Cryptosporidiosis, Leishmaniasis, Trypanosomiasis. ניתן לבדוק הדבקה טרם הטיפול מדכא החיסון ולחלק מהמחלות קיים טיפול ספציפי יעיל.
לסיכום
הסיכון לזיהומים עולה בזמן הדיכוי החיסוני, אך הסיכוי לאבחנה של הגורם המזהם בזמן החשד הקליני ולפני תחילת הטיפול, הוא נמוך מאד.
מהלך של מחלות זיהומיות בחולים מדוכאי חיסון הוא לעיתים סוער בהרבה ממהלך אותו זיהום באדם עם מערכת חיסון תקינה. הסימנים הקליניים של המחלה אינם אופייניים והאבחנה המבדלת היא רחבה וכוללת מזהמים שכיחים ואופורטוניסטים ומחלות אחרות.
לכן, הטיפול בחולים מדוכאי חיסון דורש עבודת צוות. הצוות כולל אחיות יעודיות, ורופאים מומחים מכל התחומים, המקיימים קשר הדוק ותמידי זה עם זה. הצוות צריך לספק מענה לכל בעיה שמתעוררת בזמן אמת. הזמן שחולף מהחשד הקליני לזיהום ועד לביצוע כל הבדיקות הנדרשות והתחלת הטיפול, צריך להיות קצר ביותר. בדיקות הדמיה, ביצוע ביופסיות ובדיקות אחרות הנדרשות לאבחון, צריכות להיעשות בתוך הזמן הקצר ביותר האפשרי. אבחנה מהירה וטיפול יעיל יכולים להציל חיים.
שיתוף פעולה כזה הביא לכך שמוות מספסיס בחולה מדוכא חיסון, הוא אירוע נדיר כיום, מה שמאפשר טיפול אגרסיבי יותר במחלות היסודיות עם סיכויי החלמה טובים יותר. כמובן שהמחיר לכך הוא זיהומים עם פאתוגנים חדשים ולא מוכרים.
תפקיד המומחה למחלות זיהומיות הוא להכיר את הדיכוי החיסוני, לדעת מה רמת הסיכון לזיהומים השכיחים והנדירים במצבים אלו ולהכיר הטיפולים הקיימים. הוא גם יכול לתרום להכנת החולה טרם הדיכוי החיסוני ולמניעת זיהומים בהמשך.
ד"ר רות אורני-וסרלאוף, רופאה בכירה ביחידה למחלות זיהומיות, המרכז הרפואי ע"ש סוראסקי, ת"א |