משככי כאבים אופיואידיים מהווים את בסיס הטיפול בכאב כרוני קשה שאינו ממקור סרטני, ובכאב בינוני עד קשה ממקור סרטני. למרות היעילות המוכחת בשיכוך כאבים, השימוש באופיואידים כרוך בתופעות לוואי במערכת העיכול, כאשר עצירות מדווחת כתופעת הלוואי השכיחה והממושכת ביותר, הפוגעת באופן משמעותי באיכות חייו של המטופל.
בקרב האוכלוסייה הכללית, פעילות מעיים "נורמלית" מתבטאת בלמעלה משלוש יציאות לשבוע. שכיחות העצירות באוכלוסייה הכללית היא 10 אחוז ובקרב חולי סרטן - בין 50 ל-90 אחוז, כאשר השכיחות הגבוהה ביותר היא בקרב המטופלים באופיואידים.
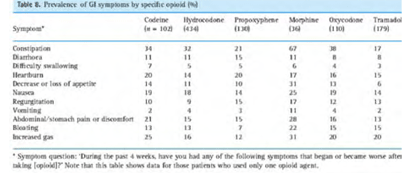
על פי סקר שנערך בארה"ב, תסמיני תפקוד מעיים לקוי דווחו על ידי חולים אשר טופלו באופיואידים בשל כאב כרוני, ללא קשר לתדירות השימוש באופיואידים. התסמינים היו ממושכים יותר עם הארכת משך הטיפול. הפרעת תפקודי מעיים בלתי נשלטת בשל שימוש באופיואידים עלולה לגרום לסיבוכים כגון: דחיסת צואה, עם שלשולים ואי שליטה בצואה; חסימת מעי, חוסר תיאבון, בחילות והקאות; הפרעה בספיגת תרופות, ואצירת ואי שליטה במתן שתן.
עצירות היא התסמין השכיח ביותר של טיפול אופיואידים. השכיחות המדווחת של עצירות בקרב חולים הסובלים מכאב כרוני שאינו ממקור סרטני והמטופלים במורפין היא 80 אחוז. חולים אלה נזקקו לתרופה אחת לפחות נגד עצירות, בעוד ש-58 אחוז נזקקו לשתי תרופות או יותר. בסדרה של 498 בתי הוספיס לטיפול בחולי סרטן סופניים, 87 אחוז ממטופלי אופיואידים נזקקו לתכשירים משלשלים.
מאחר ועצירות היא תסמין, הגדרתה היא יחסית. נוכל להעריך עצירות באמצעות שאלון הערכה (Patient Assessment of Constipation Symptom) או סולם הערכת עצירות (Constipation Assessment Scale).
עצירות חמורה עלולה להפחית את יעילותו של הטיפול בכאב באמצעות אופיואידים בלמעלה מ- 30 אחוז.
במקביל לעצירות, תסמונת קלינית שאינה מוערכת כראוי, המכונה הפרעה בתפקוד המעיים הנגרמת על ידי אופיואידים, מאופיינת כדלהלן: צואה קשה ויבשה, מאמץ, ריקון חלקי, ריבוי גזים, בטן נפוחה ורפלוקס קיבה מוגבר.
בעוד שאופיואידים הם, קרוב לוודאי, הגורם השכיח ביותר לעצירות במחלת סרטן מתקדמת, גורמים נוספים עלולים לתרום להפרעת מעיים, כגון הפרעות נוירולוגיות (הפרעת תפקוד אוטונומית ונגעים בחוט השדרה), הפרעות מטבוליות ואנדוקריניות (סוכרת, תת רמה של אשלגן, רמת יתר של סידן), סיבוכים של מחלת סרטן מתקדמת (חסימת מעיים, חוסר פעילות והתייבשות) ותרופות אחרות (תרופות אנטי- כולינרגיות, תרופות נוגדות דיכאון, תוספי ברזל/סידן ותרופות נגד יתר לחץ דם).
בסקר שנערך בארה"ב ואירופה, נותחו תוצאות שהתקבלו מ-67,189 חולים במסגרת הסקר הבינלאומי National Health and Wellness Survey (2004). הוערכו תשובות לשאלות בדבר שימוש בשירותי הבריאות, מספר ביקורים בחדר מיון, ימי אשפוז ופגיעה בתפקוד יום-יומי עבור חולים הנוטלים אופיואידים במשך שישה חודשים ומעלה, והושוו לתשובותיהם של אנשים שדיווחו או לא דיווחו על עצירות.
טבלה 1 מתארת את עלויות הטיפול בעצירות. תוצאותיו של סקר זה הראו כי מטופלים באופיואידים הסובלים מעצירות מדווחים על שימוש מוגבר בשירותי הבריאות, הגבוה באופן מובהק מזה אשר דווח על ידי אלה שאינם סובלים מעצירות.
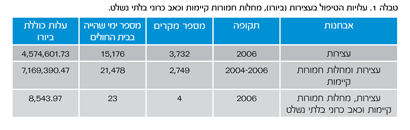
כמו כן, נטל העצירות הכרוכה בשימוש באופיואידים כלל ירידה בתפקוד והיעדרות מעבודה בעבודה בשל סבל שנגרם מעצירות.
קולטני האופיואידים במערכת העצבים המרכזית משפיעים על בקרת הכאב, בעוד שהקולטנים האופיואידים במערכת העצבים ההיקפית, כגון מערכת העיכול, גורמים למעבר מואט (ריקון מעיים דחוי), כוח דחיפה ירוד במעי הגס והדק, שינוי בתפוקה העצבית (טונוס ספינקטר אנאלי ירוד) וירידה בהפרשות המרה והמעיים.
למרות שהן למנגנון המרכזי והן למנגנון ההיקפי יש תפקיד בהשפעות האופיואידים על מערכת העיכול, עצירות הנגרמת על ידי אופיואידים כרוכה בעיקר באקטיבציה של קולטני האופיואידים המקומיים במעיים, אשר מצויים בקיבה, במעי הדק ובמעי הגס.
אקטיבציה של קולטני האופיואידים מעכבת את המסלולים העצביים המעוררים והמעכבים כאחד במערכת העצבים האנטרית, אשר מווסתת את תנועת המעיים. עיכוב המסלולים העצביים המעוררים מדכא את ההתכווצויות הפריסטלטיות, בעוד שחסימת המסלולים העצביים המעכבים גורמת להסרת העיכוב של פעילות השרירים במערכת העיכול, עלייה בטונוס השרירים במצב מנוחה, עוויתות ותנועת מעיים שאינה בכוח הדחיפה. יתרה מזו, אקטיבציה של קולטני האופיואידים גורמת לעיכוב בהפרשת מים ואלקטרוליטים, זאת בנוסף להגברה בספיגת הנוזלים ובזרימת הדם.
מניעת עצירות הנגרמת על ידי אופיואידים והפרעות בתפקוד המעיים באופן כללי, נחשבת לאסטרטגיה יעילה יותר מאשר טיפול בבעיות אלו בעת התרחשותן.
הקווים המנחים לשימור פעילות מעיים תקינה כוללים פעילות מוגברת ותנועה, עידוד צריכת נוזלים והקפדה על יציאות שגרתיות באותה השעה כל יום. ייתכן, כי העלאת כמות הסיבים התזונתיים, עצה שכיחה הניתנת לחולים, לא תהיה יעילה במיוחד, זאת מאחר שייאלצו להעלות את צריכת הסיבים שלהם ב- 450 אחוז על מנת להגביר את תדירות היציאות ב-50 אחוז.
סוגי המשלשלים העיקריים בשימוש הם סובין וצלולוז, מרככי צואה ((Docusate sodium, מעוררים bisacodyl) ו-senna), משלשלים אוסמוטיים (lactulose, sorbitol ו-Polyethylene glycol), חוקן (מי ברז ו-Sodium phosphate). ניתן להוסיף תכשירים פרוקינטיים, כגון metoclopramide, לאנשים המפתחים עמידות לטיפול במשלשלים.
התכשירים הנמצאים בשימוש כיום לטיפול בעצירות הנגרמת על ידי אופיואידים, כגון משלשלים, אינם מטפלים במנגנון הבסיסי המתווך על ידי קולטני האופיואידים ולרוב אינם יעילים. לפיכך, קיים צורך ניכר באפשרויות טיפול יעילות יותר.
אסטרטגיות חדשות וטיפולים עתידיים בעצירות בשל אופיואידים
גישה חדשנית לעיכוב סלקטיבי ומקומי של השפעות האופיואידים במערכת העיכול כרוכה במתן משולב של מעכב (אנטגוניסט) קולטני אופיואידים בעל זמינות סיסטמית זניחה, כגון naloxone פומי.
אסטרטגיה חלופית לעיכוב סלקטיבי של תופעות הלוואי של אופיואידים הפוגעות בתפקודה של מערכת העיכול היא לתת מעכבי אופיואידים בעלי ספיגה מזערית במערכת העיכול, אשר אינם עוברים בקלות את מחסום הדם-מוח.
שלושה תכשירים המהווים מעכבי קולטני אופיואידים הפועלים במערכת ההיקפית הם naloxone, methylnaltrexone ו-alvimopan.
� Methylnaltrexone הוא נגזרת quaternary N-methyl טעונה, של מעכב האופיואידים. naltrexone methylnaltrexone זמין עדיין רק בפורמולציות תת-עוריות.
� alvimopan הוא בעל מבנה רביעוני הדומה לזה של methylnaltrexone, ולפיכך הוא בעל יכולת מוגבלת לעבור את מחסום הדם-מוח. עם זאת, תוצאותיו של מחקר בטיחות ארוך טווח הראו כי הטיפול ב-alvimopan כרוך בסיכון מוגבר לאירועים קרדיווסקולאריים, בהשוואה לפלצבו. alvimopan רשום בארה"ב כתכשיר לטיפול בחסימת מעיים לאחר ניתוח, אך קיימת התוויית נגד לטיפול בו בחולים המשתמשים באופיואידים במשך למעלה מ-7 ימים.
� naloxone הוא אנטגוניסט תחרותי טהור של קולטני אופיואידים במערכות העצבים המרכזית וההיקפית, ונטול כל פעילות עצמונית של אגוניסט. בעת מתן תוך ורידי, naloxone מעכב את כל ההשפעות המתווכות על ידי אופיואידים, המרכזיות וההיקפיות כאחד. הוא עובר במהרה את מחסום הדם-מוח ולכן משמש לעתים תכופות לטיפול במינון יתר של אופיואידים. עם זאת, בעת מתן פומי, naloxone עובר פינוי נמרץ על ידי הכבד - הדבר מוביל לזמינות ביולוגית סיסטמית זניחה (פחות מ-2 אחוז).
טרם המטבוליזם בכבד, naloxone פועל באופן מקומי לעיכוב קולטני האופיואידים במעיים. מתן פומי של naloxone עשוי לאפשר חסימה סלקטיבית של קולטני האופיואידים במעיים ללא עיכוב ההשפעות הרצויות משככות הכאב של oxycodone במערכת העצבים המרכזית. naloxone הוא בעל פרופיל מוכח של בטיחות ארוכת טווח ונחשב לבטוח בטווח מינונים נרחב.
Targin היא תרופה חדשה שמשלבת אגוניסט קולטני אופיואידים חזק, oxycodone, עם אנטגוניסט קולטני אופיואידים מקומי, naloxone oxycodone מספק את אפקט שיכוך הכאב, בעוד ש-naloxone, הפועל אך ורק במעיים (בשל היותו מפונה על ידי הכבד), מונע את הופעתה של עצירות הנגרמת על ידי אופיואידים באמצעות חסימת קולטני האופיואידים במעיים. targin הוכח באופן קליני כבעל יעילות של שיכוך כאב הדומה לזו של oxycodone, לצד הפחתה משמעותית או מניעה של עצירות המושרית על ידי אופיואידים. targin הוא פורמולציה של תכשיר בשחרור ממושך, הניתן פעמיים ביום.
targin אושר לשיווק בישראל 2009 ונכלל בסל הבריאות. הוא מותווה לטיפול בכאב בינוני עד קשה ומרכיב ה-naloxone מיועד לטיפול ומניעה של עצירות הנגרמת על ידי אופיואידים.
מחקרים קליניים הראו כי חולים המטופלים ב- targin נהנים מיעילותו הטובה של oxycodone בשיכוך הכאב, לצד הקלה בעצירות המושרית על ידי אופיואידים, בהשוואה למטופלי oxycodone בלבד. targin משלב oxycodone ו-naloxone בתכשיר יחיד בעל פורמולציית שחרור איטי ומחקרים פרמקולוגיים הראו כי הוא בעל השפעה סלקטיבית וחזקה על קולטני μ ההיקפיים. מתן פומי של התכשיר מגביל את הגישה של naloxone לקולטנים המרכזיים ועד כה לא נצפו השפעות המבטלות את שיכוך הכאב או תופעות גמילה. כמו כן, נמצא כי targin משפר את תפקוד המעיים ללא משלשלים ועבור כל התרופות הללו, דיווחו המטופלים על הקלה בעצירות ושיפור כללי באיכות החיים.
מסקנות
טיפול באופיואידים כרוך, לרוב, בעצירות המגבילה את המינון ואת היכולת האנלגטית ומגבירה את אי הנוחות ופוגעת באיכות החיים. משלשלים אינם מטפלים במנגנון הבסיסי המתווך על ידי קולטני האופיואידים ולרוב אינם יעילים, וגורמים לתופעות לוואי נוספות.
חולים הסובלים מכאב כרוני עשויים להחליט על הגבלת מינון או הפסקת הטיפול באופיואידים על מנת למנוע תסמיני עצירות הנגרמים על ידם. הדבר עלול לגרום לבעיה מיוחדת אם הרופאים אינם מצליחים לצפות מראש את תופעות הלוואי של האופיואידים.
עצירות הנגרמת על ידי אופיואידים עלולה לפגוע בבקרת הכאב: 92 אחוז מהנשאלים במסגרת סקר בינלאומי, אשר הפחיתו את המינון או הפסיקו את הטיפול באופיואידים בשל עצירות, דיווחו על הגברת הכאב ופגיעה באיכות החיים ובתפקוד היומיומי. בנוסף להשפעות על החלטות החולים בדבר הטיפול באופיואידים, החששות מפני תופעות הלוואי עלולות לגרום לרופאים להימנע מרישום אופיואידים.
ההפרדה בין ההשפעות המרכזיות לבין ההשפעות ההיקפיות של קולטני האופיואידים מציעה את האפשרות למניעת העצירות המושרית על ידי אופיואידים ללא פגיעה ביעילות שיכוך הכאב, ובכך מעניקה תפיסה ייחודית של טיפול בהפרעה בתפקוד המעיים המכוון כנגד המנגנון הבסיסי.
ד"ר סילביו בריל, מנהל היחידה לטיפול בכאב, המרכז הרפואי ע"ש סוראסקי, תל אביב
ד”ר איתי גור-אריה, מנהל היחידה לשיכוך כאב, המרכז הרפואי ע"ש שיבא, תל השומר www.drpain.co.il